题目内容
13.下列实验可达到实验目的是( )①溴乙烷与NaOH的醇溶液共热充分反应后,向反应混合液中滴入酸性KMnO4 溶液,若溶液颜色变浅,则证明发生了消去反应.
②
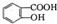 与适量NaHC03溶液反应制备
与适量NaHC03溶液反应制备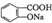
③乙酸乙酯中的少量乙酸用饱和NaOH溶液除去
④用溴水检验CH2=CH-CHO中的碳碳双键.
| A. | 只有①③④ | B. | 只有①③ | C. | 只有② | D. | 都不能 |
分析 ①乙醇能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色;
②羧基能和碳酸氢钠反应,酚羟基和碳酸氢钠不反应;
③氢氧化钠能和乙酸反应生成乙酸钠,能和乙酸乙酯反应生成乙酸钠和乙醇;
④溴能和碳碳双键发生加成反应、能和醛基发生氧化反应.
解答 解:①乙醇能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,干扰乙烯的检验,所以不能实现实验目的,故错误;
②羧基能和碳酸氢钠反应,酚羟基和碳酸氢钠不反应,所以不能实现实验目的,故错误;
③氢氧化钠能和乙酸反应生成乙酸钠,能和乙酸乙酯反应生成乙酸钠和乙醇,应该用饱和碳酸钠溶液除去乙酸乙酯中的乙酸,故错误;
④溴能和碳碳双键发生加成反应、能和醛基发生氧化反应,所以不能用溴水检验碳碳双键,故错误;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及官能团及物质检验、除杂等知识点,明确物质性质差异性是解本题关键,利用物质或官能团差异性分析解答,题目难度不大.

练习册系列答案
相关题目
4.下列各组物质的晶体中,化学键类型和晶体类型均相同的是( )
| A. | NH3和NH4Cl | B. | HCl和SiO2 | C. | CO2和H2O | D. | KCl和K |
1.下列实验操作和结论正确的是( )
| A. | 用新制Cu(0H)2悬浊液不能鉴别麦芽糖和蔗糖 | |
| B. | 硫酸铵和醋酸铅溶液均可使鸡蛋清溶液中的蛋白质变性 | |
| C. | 油是不饱和高级脂肪酸的简单甘油酯,是纯净物 | |
| D. | 用银镜反应可证明蔗糖是否转化为葡萄糖,但不能证明是否完全转化 |
8.有如下合成路线,甲经二步转化为丙:
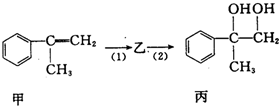
下列叙述正确的是( )
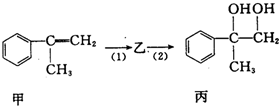
下列叙述正确的是( )
| A. | 反应(1)的无机试剂是液溴,铁作催化剂 | |
| B. | 步骤(2)产物中可能含有未反应的甲,可用酸性高锰酸钾溶液检验是否含甲 | |
| C. | 乙既能发生水解反应,又能发生消去反应 | |
| D. | 反应(1)和(2)均为取代反应 |
18.下列叙述中,错误的是( )
| A. | 苯与浓硝酸、浓硫酸水浴加热并保持55~60℃反应生成硝基苯 | |
| B. | 乙醇在浓硫酸作催化剂和脱水剂且加热至170℃时发生消去反应生成乙烯 | |
| C. | 溴乙烷在氢氧化钠醇溶液中加热发生消去反应生成乙烯 | |
| D. | 甲苯与氯气在光照下反应主要生成2,4二氯甲苯 |
5.化学在工农业生产和日常生活中都有重要应用.下列叙述正确的是( )
| A. | 葡萄糖和蛋白质等高分子化合物是人体必需的营养物质 | |
| B. | 将草木灰和硫酸铵混合施用,肥效更高 | |
| C. | 用二氧化碳生产聚碳酸酯可以减少碳排放,以减缓温室效应 | |
| D. | 棉花的主要成分是纤维素,石英玻璃、陶瓷和水泥均属于硅酸盐产品 |
2.在一密闭容器中有如下反应:aX(g)+bY(g)?nW(g),某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
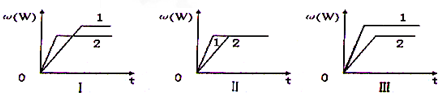
其中,ω(W)表示W在反应混合物中的体积分数,t表示反应时间.当其它条件不变时,下列分析正确的是( )

其中,ω(W)表示W在反应混合物中的体积分数,t表示反应时间.当其它条件不变时,下列分析正确的是( )
| A. | 图I可能是不同压强对反应的影响,且p2>p1,a+b>n | |
| B. | 图I可能是不同温度对反应的影响,且T2>T1,△H>0 | |
| C. | 图II可能是不同压强对反应的影响,且p1>p2,n=a+b | |
| D. | 图Ⅲ可能是不同温度对反应影响,且T1>T2,△H<0 |
3.下列离子方程式正确的是( )
| A. | 稀硝酸与氢氧化钾溶液反应 H++OH-→H2O | |
| B. | 铝与稀盐酸反应 Al+2H+→Al3++H2↑ | |
| C. | 氯化铁溶液与氢氧化钠溶液反应 FeCl3+3OH-→Fe(OH)3↓+3C1- | |
| D. | 二氧化碳与石灰水反应 CO2+2OH-→CO32-+H2O |