题目内容
3.已知:①-NO2$\stackrel{Fe+HCl}{→}$-NH2,②RBr+Mg$\stackrel{乙醚}{→}$RMgBr$→_{②H_{2}O,H+}^{①CH_{3}CHO}$
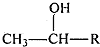
③
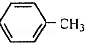 $\stackrel{KMnO_{4},H+}{→}$
$\stackrel{KMnO_{4},H+}{→}$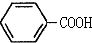
④当苯环上含有-CH3、-Cl等基团时,在苯环上新引入的基团,一般进入它们的邻位或对位,而当苯环上含有-NO2等基团时,在苯环上新引入的基团,一般进入它们的间位.某同学由烃A按下列流程进行合成实验:
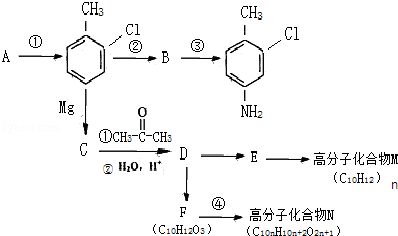
(上述流程中,D需经多步反应才能得到F,在此不作要求)
(1)由A合成B可有两种途径,除题中生成中间产物
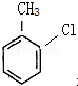 这一途径外,另一途径生成的中间产物的结构简式为
这一途径外,另一途径生成的中间产物的结构简式为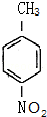 ,假定每次反应所得可能产物的机会是均等的,试分析,当消耗等量反应物时题中(填“题中”或“另一”)途径获得B的产量更高;
,假定每次反应所得可能产物的机会是均等的,试分析,当消耗等量反应物时题中(填“题中”或“另一”)途径获得B的产量更高;(2)反应①的条件为铁粉作催化剂,反应②所用试剂混合的先后顺序为先加浓硝酸后加浓硫酸,反应④的反应类型为缩聚反应,D的核磁共振氢谱有6条峰;
(3)写出生成高分子化合物N的化学方程式n
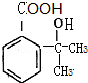 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$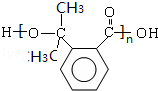 +(n-1)H2O;
+(n-1)H2O;(4)写出一种符合下列三个条件的有机物的结构简式
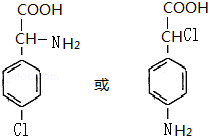 等.
等.①分子式比B多一个“CH2”,②具有“两性”,③苯环上的一氯代物只有两种.
分析 根据题中各物质转化关系,A与氯气发生苯环上的取代生成 ,则A为
,则A为 ,反应条件应为铁粉做催化剂,比较
,反应条件应为铁粉做催化剂,比较 和
和 的结构,可知B为
的结构,可知B为 ,反应②为硝化反应,
,反应②为硝化反应, 与镁反应生成C为
与镁反应生成C为 ,根据题中信息②可知D为
,根据题中信息②可知D为 ,根据F的分子式以及生成高分子化合物N的分子式可知,F为
,根据F的分子式以及生成高分子化合物N的分子式可知,F为 ,N为
,N为 ,F发生缩聚反应生成N,
,F发生缩聚反应生成N,
据此分析解答.
解答 解:根据题中各物质转化关系,A与氯气发生苯环上的取代生成 ,则A为
,则A为 ,反应条件应为铁粉做催化剂,比较
,反应条件应为铁粉做催化剂,比较 和
和 的结构,可知B为
的结构,可知B为 ,反应②为硝化反应,
,反应②为硝化反应, 与镁反应生成C为
与镁反应生成C为 ,根据题中信息②可知D为
,根据题中信息②可知D为 ,根据F的分子式以及生成高分子化合物N的分子式可知,F为
,根据F的分子式以及生成高分子化合物N的分子式可知,F为 ,N为
,N为 ,F发生缩聚反应生成N,
,F发生缩聚反应生成N,
(1)由A合成B可有两种途径,除题中生成中间产物 这一途径外,另一途径生成的中间产物的结构简式为
这一途径外,另一途径生成的中间产物的结构简式为  ,假定每次反应所得可能产物的机会是均等的,由于甲苯与硝酸反应硝基也有可能取代在甲基的邻位上,且有两个邻位可取代,所以当消耗等量反应物时题中途径获得B的产量更高,
,假定每次反应所得可能产物的机会是均等的,由于甲苯与硝酸反应硝基也有可能取代在甲基的邻位上,且有两个邻位可取代,所以当消耗等量反应物时题中途径获得B的产量更高,
故答案为: ;题中;
;题中;
(2)根据上面的分析可知,反应①的条件为铁粉做催化剂,反应②为硝化反应,要用浓硫酸作催化剂,所用试剂混合的先后顺序为先加浓硝酸再加浓硫酸,反应④的反应类型为缩聚反应,D为 ,D的核磁共振氢谱有6条峰,
,D的核磁共振氢谱有6条峰,
故答案为:铁粉做催化剂;先加浓硝酸再加浓硫酸;缩聚反应;6;
(3)生成高分子化合物N的化学方程式为n

 +(n-1)H2O,
+(n-1)H2O,
故答案为:n

 +(n-1)H2O;
+(n-1)H2O;
(4)B为 ,符合下列三个条件①分子式比B多一个“CH2”,②具有“两性”,③苯环上的一氯代物只有两种,这样的有机物的结构简式为
,符合下列三个条件①分子式比B多一个“CH2”,②具有“两性”,③苯环上的一氯代物只有两种,这样的有机物的结构简式为 等,故答案为:
等,故答案为: 等.
等.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及知识综合运用能力,把握物质结构特点及其性质是解本题关键,注意题给信息的灵活运用,题目难度中等.

练习册系列答案
相关题目
14.在 分子中,处于同一平面上的碳原子数最多可能有( )
分子中,处于同一平面上的碳原子数最多可能有( )
 分子中,处于同一平面上的碳原子数最多可能有( )
分子中,处于同一平面上的碳原子数最多可能有( )| A. | 6个 | B. | 8个 | C. | 10个 | D. | 12个 |
11.下列关于加热的操作正确的是( )
| A. | 给试管中的液体加热时,试管口不准对着别人,但可以对着自己 | |
| B. | 玻璃仪器都可以用于加热 | |
| C. | 在H2还原氧化铜的实验中,应把H2通过预先加热的氧化铜 | |
| D. | 无论给试管中的液体还是固体加热,都必须先预热 |
18.若NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2LSO3所含原子数为2NA | |
| B. | 标况下11.2LNO和11.2LO2混合后所得气体分子数为NA | |
| C. | 0.1mol•L-1的NaHSO4溶液中,阳离子的数目之和为0.2NA | |
| D. | 1mol SiO2晶体中含有硅氧键的数目为4NA.而1mol金刚石中含碳碳键的数目为2NA |
15.电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2 ( )2L


| A. | 大于 | B. | 小于 | C. | 等于 | D. | 不能确定 |
12.经测定,某集气瓶中只含N和O两种元素,下列说法不正确的是( )
| A. | 集气瓶中所含物质可能是纯净物 | |
| B. | 集气瓶中可能只含有两种单质 | |
| C. | 集气瓶中不可能既存在单质又存在化合物 | |
| D. | 集气瓶中可能含有一种单质和一种化合物 |