题目内容
18.将2mol•L-1的盐酸10mL逐滴滴加到20mL某浓度的NaOH溶液中,恰好完全反应,试计算该NaOH溶液中含有NaOH的质量是多少克?分析 已知2mol•L-1的盐酸10mL,则n(HCl)=2mol/L×0.01L=0.02mol,根据HCl与NaOH的反应关系计算NaOH的物质的量,再根据m=nM计算.
解答 解:已知2mol•L-1的盐酸10mL,则n(HCl)=2mol/L×0.01L=0.02mol,HCl与NaOH恰好完全反应,则n(NaOH)=0.02mol,
所以m(NaOH)=nM=0.02mol×40g/mol=0.8g;
答:含有NaOH的质量是0.8g.
点评 本题考查化学方程式的有关计算,题目难度不大,侧重考查学生分析计算能力,注意把握反应方程式中各物质之间的关系以及物质的量的计算公式.

练习册系列答案
相关题目
9.(1)写出下列基团的名称:
(2)写出下列有机物的系统命名或结构简式:
①
②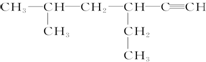
③2,2-二甲基-3-乙基己烷④2-甲基-2-丁烯.
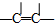 | ─C≡C─ | ─CH3 | ─CH2CH3 或─C2H5 | ─OH | ─CHO | ─COOH | -COO-R |
①

②

③2,2-二甲基-3-乙基己烷④2-甲基-2-丁烯.
13.保护环境已成为人类的共识,下列做法不利于环境保护的是( )
| A. | 火力发电厂的煤经粉碎、脱硫处理 | B. | 电镀废液经中和后直接排入到农田 | ||
| C. | 聚乳酸塑料代替传统塑料作购物袋 | D. | 回收并合理处理聚氯乙烯塑料废物 |
3.下列关于水污染叙述错误的是( )
| A. | 水污染的程度是由其溶氧量来测定 | |
| B. | 污染水的金属元素如汞、镉、铅等的含量极少时,不会对生物造成伤害 | |
| C. | 使用含磷洗衣粉会造成河水、湖水污染,使海藻疯狂生长,鱼类死亡 | |
| D. | 工业所排出的废水危害水生生物 |
10.下列关于阿伏加德罗常数的说法正确的是( )
| A. | 阿伏加德罗常数是12 g碳中所含的碳原子数 | |
| B. | 24 g镁的原子最外层电子数为NA | |
| C. | 阿伏加德罗常数约是6.02×1023 | |
| D. | 阿伏加德罗常数的符号为NA,近似为6.02×1023 mol-1 |
7.在相同温度时,100mL 0.01mol/L的醋酸溶液与10mL 0.1mol/L的醋酸溶液相比较,下列数值前者大于后者的是( )
| A. | 中和时所需NaOH的量 | B. | 电离的程度 | ||
| C. | H+的物质的量浓度 | D. | H+的物质的量 |
8.下列混合物的分离或提纯操作不正确的是( )
| A. | 除去N2中的少量O2,可通过灼热的Cu网后,收集气体 | |
| B. | 除去FeCl3溶液中Fe(OH)3沉淀可以过滤 | |
| C. | 除去乙醇中的少量NaCl,可用蒸馏的方法 | |
| D. | 重结晶不能用于提纯物质 |
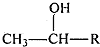
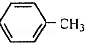 $\stackrel{KMnO_{4},H+}{→}$
$\stackrel{KMnO_{4},H+}{→}$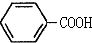
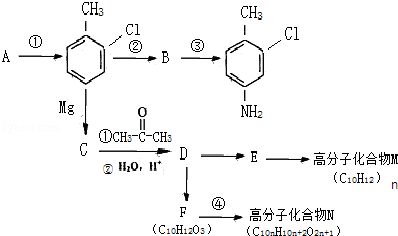
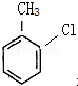 这一途径外,另一途径生成的中间产物的结构简式为
这一途径外,另一途径生成的中间产物的结构简式为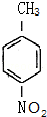 ,假定每次反应所得可能产物的机会是均等的,试分析,当消耗等量反应物时题中(填“题中”或“另一”)途径获得B的产量更高;
,假定每次反应所得可能产物的机会是均等的,试分析,当消耗等量反应物时题中(填“题中”或“另一”)途径获得B的产量更高;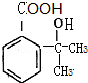 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$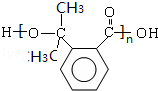 +(n-1)H2O;
+(n-1)H2O;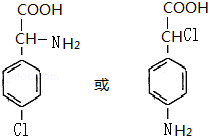 等.
等.