题目内容
用已知浓度的盐酸滴定未知浓度的NaOH溶液会导致测得的NaOH溶液浓度偏高的是( )
| A、滴定前滴定管中无气泡,滴定后产生气泡 |
| B、碱式滴定管量取NaOH溶液时,未进行润洗操作 |
| C、滴定时达到滴定终点时仰视读数 |
| D、锥形瓶盛装NaOH待测液前加少量水洗涤 |
考点:中和滴定
专题:电离平衡与溶液的pH专题
分析:根据c(待测)=
分析不当操作对V(标准)的影响,以此判断浓度的误差;
| c(标准)×V(标准) |
| V(待测) |
解答:
解:A.滴定前滴定管中无气泡,滴定后产生气泡,造成V(标准)偏小,根据c(待测)=
分析可知c(待测)偏小,故A错误;
B.碱式滴定管用蒸馏水洗净后,直接加入NaOH溶液,导致待测液浓度减小,故B错误;
C.滴定前读数正确,达到滴定终点后,仰视读数,导致V(标准)偏大,根据c(待测)=
分析可知c(待测)偏大,故C正确;
D.锥形瓶盛装NaOH待测液前加少量水洗涤,待测液的物质的量不变,标准液的体积不变,结果不变,故D错误;
故选C.
| c(标准)×V(标准) |
| V(待测) |
B.碱式滴定管用蒸馏水洗净后,直接加入NaOH溶液,导致待测液浓度减小,故B错误;
C.滴定前读数正确,达到滴定终点后,仰视读数,导致V(标准)偏大,根据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
D.锥形瓶盛装NaOH待测液前加少量水洗涤,待测液的物质的量不变,标准液的体积不变,结果不变,故D错误;
故选C.
点评:本题主要考查了中和滴定操作的误差分析,根据c(待测)=
分析是解答的关键,题目难度中等.
| c(标准)×V(标准) |
| V(待测) |

练习册系列答案
相关题目
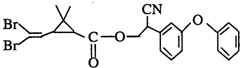 拟除虫菊酯是一类高效、低毒、对昆虫 具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如右图:下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫 具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如右图:下列对该化合物叙述正确的是( )| A、属于芳香烃 |
| B、分子中含有4个手性碳 |
| C、含有3种官能团 |
| D、能发生取代、加成、加聚、氧化、消去反应 |
在某恒定温度下,向容积为1L的容器中投入1mol CO和2mol H2O,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),平衡时生成CO2
mol.若保持温度和容积不变,向其中增加2mol H2O(g),使反应到达新的平衡,下列说法不正确的是( )
| 2 |
| 3 |
| A、新、旧平衡时容器内气体的压强之比是5:3 |
| B、新平衡时H2O的转化率为20% |
| C、新平衡时CO的浓度是0.2 mol?L-1 |
| D、新、旧平衡时容器内气体密度之比为5:3 |
用某种仪器量取液体体积时,平视时读数为nmL,仰视时读数为x mL,俯视时读数为y mL,若X>n>y,则所用的仪器可能为( )
| A、量筒 | B、容量瓶 |
| C、滴定管 | D、以上均不对 |