题目内容
18.用NA表示阿伏伽德罗常数的值,下列有关说法中正确的是( )| A. | 200mL 2mol/L蔗糖溶液中所含分子数为0.4NA | |
| B. | 标准状况下,2.24L HF的氢原子数目为0.1 NA | |
| C. | 黑火药爆炸的方程式为2KNO3+3C+S═K2S+N2↑+3CO2↑,当生成1molK2S时转移电子数为2NA | |
| D. | 标准状况下,1.12L 1H2和0.2g2H2均含有0.1 NA质子 |
分析 A、蔗糖溶液中除了蔗糖分子,还有水分子;
B、标况下HF为液体;
C、反应2KNO3+3C+S═K2S+N2↑+3CO2↑转移12mol电子;
D、分别求出标准状况下,1.12L 1H2和0.2g2H2的物质的量,然后根据1H2和2H2中均含2个质子来分析.
解答 解:A、蔗糖溶液中除了蔗糖分子,还有水分子,故溶液中的分子个数大于0.4NA个,故A错误;
B、标况下HF为液体,故不能根据气体摩尔体积来计算其物质的量和含有的原子个数,故B错误;
C、反应2KNO3+3C+S═K2S+N2↑+3CO2↑转移12mol电子,生成1mol硫化钾,故当生成1mol硫化钾时转移12mol电子即12NA个,故错误;
D、标准状况下,1.12L 1H2的物质的量为0.05mol,0.2g2H2的物质的量也为0.05mol,而1H2和2H2中均含2个质子,故0.05mol两者中含有的质子数均为0.1NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
8.短周期元素X、Y、Z、W、M的原子序数依次增大,其中X、W同主族,Y+与X2-具有相同的电子层结构;离子半径:W2->M-,Z的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法正确的是( )
| A. | 原子最外层电子数:X>Y>Z | |
| B. | 原子半径:X>Y>Z | |
| C. | 最高价氧化物对应水化物的酸性:W>Z | |
| D. | 最简单气态氢化物的稳定性:X>W>M |
9.下列离子方程式中,正确的是( )
| A. | 氯化铁溶液腐蚀印刷线路板:Fe3++Cu=Fe2++Cu2+ | |
| B. | 将少量铜屑放入浓硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O | |
| C. | 钠和水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 碳酸氢钠溶液与盐酸反应:CO32-+2H+=CO2↑+H2O |
6.已知常温下浓度为0.1mol•L-1的下列溶液的pH如表所示:
下列有关说法正确的是( )
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A. | 0.1 mol•L-1 Na2CO3溶液中,存在关系:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| B. | 加热0.1 mol•L-1 NaClO溶液测其pH,pH小于9.7 | |
| C. | pH=2的HF溶液与pH=12的NaOH溶液以等体积混合,则有c(Na+)=c(F-)>c(H+)=c(OH-) | |
| D. | 根据上表数据得出三种酸电离平衡常数大小关系为:HF>HClO>H2CO3(一级电离平衡常数) |
13. 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
实验仪器
I.实验原理:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O.
Ⅱ.实验设计
(1)【方案】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4
溶液混合后,溶液褪色所需的时间.拟定实验数据:
表中①、②处的数据分别是25、7.0.
III.讨论与交流
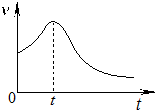
(2)小组同学在处理一系列的实验数据时,发现速率(v)-时间(t)曲线如图所示.他们认为:0~t时间内,速率变快的可能原因是①产物Mn2+是反应的催化剂、②该反应放热使温度升高.
(3)实验室常用KMnO4标准溶液滴定某浓度草酸.
KMnO4溶液置于酸式滴定管(填仪器名称)中,判断到达滴定终点的现象是溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.实验仪器
I.实验原理:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O.
Ⅱ.实验设计
(1)【方案】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4
溶液混合后,溶液褪色所需的时间.拟定实验数据:
| 实验序号 | 温度/℃ | 各物质的体积/mL | 反应时间 | |||
| H2O | 3mol/L稀硫酸 | 0.1mol/L KMnO4溶液 | 0.6mol/LH2C2O4溶液 | |||
| 1 | 25 | 3.0 | 2.0 | 4.0 | 6.0 | t1 |
| 2 | ① | 5.0 | 2.0 | 4.0 | 4.0 | t2 |
| 3 | 25 | ② | 2.0 | 4.0 | 2.0 | t3 |
III.讨论与交流
(2)小组同学在处理一系列的实验数据时,发现速率(v)-时间(t)曲线如图所示.他们认为:0~t时间内,速率变快的可能原因是①产物Mn2+是反应的催化剂、②该反应放热使温度升高.
(3)实验室常用KMnO4标准溶液滴定某浓度草酸.
KMnO4溶液置于酸式滴定管(填仪器名称)中,判断到达滴定终点的现象是溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L H2 与O2的混合气体所含原子数为2NA | |
| B. | 标准状况下,18g H2O的体积是22.4L | |
| C. | NA个SO2的体积是22.4L | |
| D. | 在常温、常压下,11.2L N2含有的分子数为0.5NA |
7.铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等.

(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观.指明使用镁条和氯酸钾的目的是引发铝热反应.(不超过8个字)
(2)某同学用图乙装置进行铝热反应.取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色.为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示.
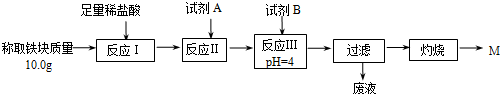
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示.
①试剂A应选择C,试剂B应选择D.(填序号)
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
②写出反应Ⅱ的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O
③设计简单实验证明M的成分是Fe2O3而非Fe3O4.
【限选试剂:稀盐酸、稀硫酸、氯水、高锰酸钾溶液、KSCN溶液、双氧水】
④上述实验应灼烧至M质量不变,则能证明M质量不变的标志是连续两次灼烧质量相差不大于0.1g.
⑤若最终红色粉未M的质量为12.0g,则该“铁块”的纯度是84%.

(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观.指明使用镁条和氯酸钾的目的是引发铝热反应.(不超过8个字)
(2)某同学用图乙装置进行铝热反应.取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色.为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示.

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示.
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
②写出反应Ⅱ的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O
③设计简单实验证明M的成分是Fe2O3而非Fe3O4.
【限选试剂:稀盐酸、稀硫酸、氯水、高锰酸钾溶液、KSCN溶液、双氧水】
| 操作 | 预期现象 |
| 取少量M固体于试管中,向其中加入足量稀硫酸;观察. | 固体完全溶解,溶液呈黄色. |
继续向上述溶液中滴入几滴(少量)高锰酸钾溶液,振荡观察 | 溶液紫红色未褪去 |
⑤若最终红色粉未M的质量为12.0g,则该“铁块”的纯度是84%.
8.下列实验操作或处理正确的是( )
| A. | 将NaOH溶液逐滴加入饱和的FeCl3溶液中制取Fe(OH)3胶体 | |
| B. | 氯气泄漏后应顺风向低处跑 | |
| C. | 金属钠着火立刻用湿布盖灭 | |
| D. | 做完焰色反应实验的铂丝用稀盐酸清洗 |
 现有含有少量KCl、K2SO4、K2CO3杂质的KNO3溶液,选择适当的试剂除去杂质,得到纯净的KNO3固体,实验流程如图所示.
现有含有少量KCl、K2SO4、K2CO3杂质的KNO3溶液,选择适当的试剂除去杂质,得到纯净的KNO3固体,实验流程如图所示.