题目内容
18.A、B、C、D、E代表周期表中五种短周期元素,已知:①A、B、C处于相邻位置,B、C同周期,A、B同主族,其核外电子数之和为41.②D与C处于周期表中同一周期,D+中各层电子数都是2n2个.③A、B、C、D、E各元素最外层电子数之和 23,且已知B、D、E三种元素的最高价氧化物的水化物之间相互都能反应生成盐和水.据此填空下列空白:(用元素符号或化学式表示)(1)元素A为OD为Na E为Al 元素C的某种原子的中子数比质子数多3个,表示该原子组成的符号为3717Cl
(2)A、B、C、D的离子半径由大到小的顺序:S 2->Cl->O 2->Na+
(3)A、B、C的氢化物的稳定性由强到弱的顺序:H2O>HCl>H2S
(4)化合物BA2与C单质的水溶液反应的化学方程式:SO2+Cl2+2H2O=H2SO4+2HCl
(5)由A、E组成的化合物与质子结合的离子方程式:Al2O3+6H+=2Al3++3H2O.
分析 A、B、C、D、E代表周期表中五种短周期元素,D+中各层电子数都是2n2个,且为短周期元素,则D是Na元素;C和D处于同一周期、B和C同一周期,则B、C都位于第三周期,A和B同一主族,则A位于第二周期,A、B、C处于相邻位置,A、B、C核外电子数之和为41,设A原子序数是a(a为正整数),则B原子序数为a+8,C原子序数为a+7或a+9,则a+a+8+a+7=41,故a=$\frac{26}{3}$(舍去),a+a+8+a+9=41,则a=8,则A是O元素、B是S元素、C是Cl元素;A、B、C、D、E各元素最外层电子数之和 23,E原子最外层电子数为23-6-6-7-1=3,且B、D、E三种元素的最高价氧化物的水化物之间相互都能反应生成盐和水,可推知E为Al.
解答 解:A、B、C、D、E代表周期表中五种短周期元素,D+中各层电子数都是2n2个,且为短周期元素,则D是Na元素;C和D处于同一周期、B和C同一周期,则B、C都位于第三周期,A和B同一主族,则A位于第二周期,A、B、C处于相邻位置,A、B、C核外电子数之和为41,设A原子序数是a(a为正整数),则B原子序数为a+8,C原子序数为a+7或a+9,则a+a+8+a+7=41,故a=$\frac{26}{3}$(舍去),a+a+8+a+9=41,则a=8,则A是O元素、B是S元素、C是Cl元素;A、B、C、D、E各元素最外层电子数之和 23,E原子最外层电子数为23-6-6-7-1=3,且B、D、E三种元素的最高价氧化物的水化物之间相互都能反应生成盐和水,可推知E为Al.
(1)由上述分析可知,A为O元素、D为Na元素、E为Al,C为Cl,元素C的某种原子的中子数比质子数多3个,质量数为17+17+3=37,表示该原子组成的符号为3717Cl,
故答案为:O;Na;Al;3717Cl;
(2)A、B、C、D离子分别是O 2-、S 2-、Cl-、Na+,离子电子层越多,离子半径越大,电子层结构相同的离子,核电荷数越大,离子半径越小,故离子半径:S 2->Cl->O 2->Na+,
故答案为:S 2->Cl->O 2->Na+;
(2)元素的非金属性越强,其氢化物的稳定性越强,非金属性O>Cl>S,所以氢化物的稳定性:H2O>HCl>H2S,故答案为:H2O>HCl>H2S;
(4)化合物SO2与氯气在水溶液中发生氧化还原反应生成硫酸和HCl,反应方程式为:SO2+Cl2+2H2O=H2SO4+2HCl,故答案为:SO2+Cl2+2H2O=H2SO4+2HCl;
(5)由A、E组成的化合物为Al2O3,与质子结合的离子方程式:Al2O3+6H+=2Al3++3H2O,
故答案为:Al2O3+6H+=2Al3++3H2O.
点评 本题考查位置结构性质相互关系及应用,推断元素是解题关键,侧重考查学生推理能力、元素周期律等,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 绿色化学的核心是应用化学原理治理产生的环境污染 | |
| B. | 采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 | |
| C. | 采用天然石材装修家居,可减轻室内甲醛污染但会导致一定量的放射性物质的污染 | |
| D. | PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越高,大气污染越严重 |
| A. | ①红色褪去的原因是KMnO4将SCN-氧化,使Fe(SCN)3消失 | |
| B. | ②红色褪去的原因是SO2将Fe3+还原为Fe2+ | |
| C. | ②红色褪去的原因是SO2将SCN-还原 | |
| D. | SCN-在适当条件下可失去电子被氧化剂氧化为(SCN)2 |
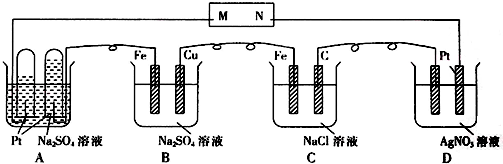
以下有关的推断中正确的( )
①M是电源的负极 ②B中Cu电极的质量减少 ③C中溶液的pH升高
④D中溶液的pH下降 ⑤B中一段时间后溶液出现蓝色沉淀
⑥相同条件下的A,C,D池中生成气体的总体积为C>A>D.
| A. | 只有⑤⑥ | B. | 只有③④⑤⑥ | C. | 全部 | D. | 除② |
| A. | 离子的氧化性:Y>Z | B. | 氢化物的沸点:X<W | ||
| C. | X、W最高正价相同 | D. | 原子及离子半径:Z>Y>X |
| A. | 1:2 | B. | 1:3 | C. | 1:1 | D. | 2:1 |
| A. | 第3周期第ⅠA族 | B. | 第4周期第ⅠA族 | C. | 第5周期第ⅠA族 | D. | 第3周期第ⅡA族 |