题目内容
9.在28%的KOH水溶液中,OH-离子与H2O分子数之比是1:8.分析 设溶液质量为100g,则KOH为28g,水为100g-28g=72g,根据n=$\frac{n}{M}$计算解答.
解答 解:设溶液质量为100g,则KOH为28g,水为100g-28g=72g,
n(OH-)=n(KOH)=$\frac{28g}{56g/mol}$=0.5mol,
n(H2O)=$\frac{72g}{18g/mol}$=4mol,
故溶液中n(OH-);n(H2O)=0.5mol:4mol=1:8
故答案为:1:8.
点评 本题考查物质的量有关计算,比较基础,注意利用赋值法进行解答.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
19.下列变化属于氧化还原反应的是( )
| A. | 馒头在咀嚼过程中产生甜味 | |
| B. | 三氯化铁溶液长期放置产生红褐色固体 | |
| C. | 蛋白质溶液中加入饱和硫酸铵溶液,析出沉淀 | |
| D. | 植物油长期放置发生“酸败产生刺激性气味” |
20.下列反应属于吸热反应的是( )
| A. | 氢氧化钡与盐酸溶液反应 | B. | 葡萄糖在人体内氧化分解 | ||
| C. | 石灰石在高温下的分解反应 | D. | 锌粒与稀H2SO4反应制取H2 |
17.A、B、C、D、E、F、G为由七种短周期元素构成的粒子,它们都有10个电子,其结构特点如下表:
其中,B的离子半径大于E的离子半径;D是常温常压下能使湿润红色石蕊试纸变蓝色的气体;C常用作F的检验(加热).请填写下列空白:
(1)A粒子的结构示意图 ,G的化学式是CH4.
,G的化学式是CH4.
(2)比较BC和EC2的碱性强弱BC>EC2(填<、>、=).
(3)F与C反应生成D的离子方程式NH4++OH-=NH3.H2O.
| 粒子代号 | A | B | C | D | E | F | G |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
(1)A粒子的结构示意图
 ,G的化学式是CH4.
,G的化学式是CH4.(2)比较BC和EC2的碱性强弱BC>EC2(填<、>、=).
(3)F与C反应生成D的离子方程式NH4++OH-=NH3.H2O.
14.已知:
CH3CH2CH2CH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2878kJ/mol
(CH3)2CHCH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2869kJ/mol
下列说法正确的是( )
CH3CH2CH2CH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2878kJ/mol
(CH3)2CHCH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2869kJ/mol
下列说法正确的是( )
| A. | 正丁烷的稳定性大于异丁烷 | |
| B. | 异丁烷分子中的碳氢键比正丁烷的多 | |
| C. | 等物质的量的正丁烷能量大于异丁烷能量 | |
| D. | 异丁烷转化为正丁烷的过程是一个放热过程 |
19.A原子的结构示意图为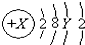 .则下列说法正确的是( )
.则下列说法正确的是( )
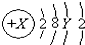 .则下列说法正确的是( )
.则下列说法正确的是( )| A. | 3p能级上的电子数只能为6 | |
| B. | 3d能级上的电子数可能为1-10 | |
| C. | Y可只能为3-8 | |
| D. | 2p,3p能级上的电子数可以相同,也可以不同 |
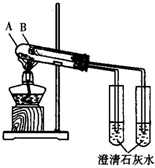 研究Cl2、SO2、CO2、NH3等气体的性质对生产和生活与重要的意义.
研究Cl2、SO2、CO2、NH3等气体的性质对生产和生活与重要的意义.