题目内容
3mol氧分子的质量为 .
考点:物质的量的相关计算
专题:
分析:根据m=nM计算.
解答:
解:m=nM=3mol×32g/mol=96g,
故答案为:96g.
故答案为:96g.
点评:本题考查物质的量的计算,为高频考点,侧重学生的分析、计算能力的考查,注意把握相关计算公式,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有关AgCl沉淀的溶解平衡说法正确的是( )
| A、AgCl沉淀生成和溶解不断进行,但速率相等 |
| B、AgCl难溶于水,其溶液中没有Ag+和Clˉ |
| C、升高温度,AgCl沉淀的溶解度不变 |
| D、向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度不变 |
 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),p(CO32-)=-lgc(CO32-).下列说法正确的是( )
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),p(CO32-)=-lgc(CO32-).下列说法正确的是( )| A、MgCO3、CaCO3、MnCO3的Ksp依次增大 |
| B、a点可表示MnCO3的饱和溶液,且c(Mn2+)<c(CO32-) |
| C、b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D、c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-) |
向含有0.010mol?L-1 CrO42-离子和0.010mol?L-1 SO42-离子的混合溶液中,逐滴加入少量Pb(NO3)2溶液(忽略加入Pb(NO3)2所引起的体积变化),下列说法正确的是(KSP (PbCrO4)=2.8×10-13,KSP (PbSO4)=2.8×10-8)( )
| A、PbCrO4先沉淀 |
| B、PbSO4先沉淀 |
| C、PbCrO4和PbSO4一起沉淀 |
| D、PbCrO4和PbSO4都不沉淀 |
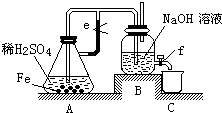
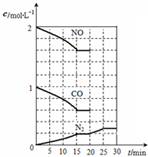 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.