题目内容
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、将1molCl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA | ||
| B、常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA | ||
| C、标准状况下,2.24L的CCl4中含有的C-Cl键数为0.4NA | ||
D、将CO2通过Na2O2使其增重a克时,反应中转移电子数为
|
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据氯原子的守恒来分析;
B、甲醛和冰醋酸的最简式为CH2O,3.0g混合物中含有0.1mol最简式;
C、标况下,四氯化碳为液态;
D、根据Na2O2与CO2的反应分析可知,转移2mol电子时,增重2molCO的质量.
B、甲醛和冰醋酸的最简式为CH2O,3.0g混合物中含有0.1mol最简式;
C、标况下,四氯化碳为液态;
D、根据Na2O2与CO2的反应分析可知,转移2mol电子时,增重2molCO的质量.
解答:
解:A.1mol氯气中共含2mol氯原子,而氯气与水的反应为可逆反应,不能进行彻底,故溶液中有HClO分子、ClO-、Cl-、Cl2分子,根据氯原子的守恒可有:2NA=N(HClO)+N(Cl-)+N(ClO-)+2N(Cl2),即N(HClO)+N(Cl-)+N(ClO-)=2[NA-N(Cl2)],故A错误;
B.3.0g含甲醛的冰醋酸中含有0.1mol最简式CH2O,含有0.4mol原子,含有的原子总数为0.4NA,故B正确;
C、CCl4在标准状况下为液体,不能用气体摩尔体积进行计算,故C错误;
D.根据Na2O2与CO2的反应分析可知,转移2mol电子时,增重2molCO的质量即56g,故当增重a克时,即转移
mol电子,即
个,故D错误.
故选B.
B.3.0g含甲醛的冰醋酸中含有0.1mol最简式CH2O,含有0.4mol原子,含有的原子总数为0.4NA,故B正确;
C、CCl4在标准状况下为液体,不能用气体摩尔体积进行计算,故C错误;
D.根据Na2O2与CO2的反应分析可知,转移2mol电子时,增重2molCO的质量即56g,故当增重a克时,即转移
| a |
| 28 |
| aNA |
| 28 |
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
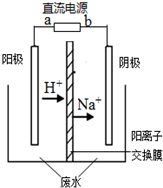 最近有研究人员利用隔膜电解法处理高浓度的乙醛废水.乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法不正确的是( )
最近有研究人员利用隔膜电解法处理高浓度的乙醛废水.乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法不正确的是( )| A、电解过程中,阴极附近的乙醛被氧化 |
| B、阳极反应CH3CHO-2e-+H2O═CH3COOH+2H+ |
| C、若以CH4-空气燃料电池为直流电源,燃料电池的b极应通入CH4 |
| D、现处理含1mol乙醛的废水,至少需转移1mol电子 |
化学与生产生活、环境保护密切相关.下列说法中不正确的是( )
| A、食盐既可作调味品也可作食品防腐剂 |
| B、向海水中加入净水剂明矾可以使海水淡化 |
| C、加大石油、煤炭的开采速度,增加化石燃料的供应不利于“蓝天工程”的建设 |
| D、高铁车厢材料大部分采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强 |
下列说法正确的是( )
| A、只含一种分子的物质是纯净物,只含一种元素的物质也是纯净物 |
| B、酸的分子式中有几个氢就是几元酸 |
| C、金刚石、石墨、C60互为同素异形体 |
| D、C、N、O三种元素的第一电离能:C<N<O;电负性:C<N<O |
NA为阿伏伽德罗常数,下列叙述正确的是( )
| A、18gH2O中含有的质子数为NA |
| B、常温常压下,Na2O2与足量H2O反应,每生成1 molO2,转移电子的数目为4NA |
| C、46gNO2和N2O4混合气体中含有原子总数为3NA |
| D、物质的量浓度为0.5 mol?L-1的MgCl2的溶液中,含有Cl-个数为NA |
设NA为阿伏加德罗常数的值,N表示粒子数.下列说法正确的是( )
| A、0.1 mol苯乙烯中含有碳碳双键的数目为0.4NA |
| B、将1molCl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2[NA-N(Cl2)] |
| C、一定条件下,0.1 mol SO2与足量氧气反应生成SO3,转移电子数为0.2NA |
| D、电解精炼铜,当电路中通过的电子数目为0.2NA时,阳极质量减少6.4g |
下列化学用语的表示正确的是( )
A、CS2的比例模型: |
| B、乙醇的结构简式:C2H6O |
| C、核内有8个中子的碳原子:86C |
| D、HClO的结构简式:H-Cl-O |
下列各组物质中,化学键类型不同的是( )
| A、NaCl和HNO3 |
| B、H2O和NH3 |
| C、CaF2和CsCl |
| D、CCl4和HCl |
下列关于浓硫酸的相关实验叙述中正确的是.
| A、在浓硫酸和Cu的实验中,反应后试管里没有明显的颜色变化,为了确定生成物可以往试管里加入少量水,观察颜色变化. |
| B、在浓硫酸和Cu的实验中,反实验结束停止加热后,可将导管口插入蘸有NaOH溶液的棉花团中吸收尾气 |
| C、在蔗糖炭化的实验中,会闻到有刺激性气味的气体,该气体主要是SO2 |
| D、在浓硫酸和Cu的实验中,将产生的气体通入石蕊试液中,发现溶液先变红,后褪色 |