题目内容
下列说法正确的是( )
| A、只含一种分子的物质是纯净物,只含一种元素的物质也是纯净物 |
| B、酸的分子式中有几个氢就是几元酸 |
| C、金刚石、石墨、C60互为同素异形体 |
| D、C、N、O三种元素的第一电离能:C<N<O;电负性:C<N<O |
考点:混合物和纯净物,同素异形体,酸、碱、盐、氧化物的概念及其相互联系,元素电离能、电负性的含义及应用
专题:
分析:A、纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质;
B、一个酸分子电离出n个氢离子,该酸为n元酸,含氧酸中含几个羟基氢原子则为几元酸,据此解答即可;
C、由同种元素组成的不同单质,互称为同素异形体;
D、同周期元素从左到右元素的第一电离能逐渐增大,但是N存在2p轨道上的半充满状态,据此判断.
B、一个酸分子电离出n个氢离子,该酸为n元酸,含氧酸中含几个羟基氢原子则为几元酸,据此解答即可;
C、由同种元素组成的不同单质,互称为同素异形体;
D、同周期元素从左到右元素的第一电离能逐渐增大,但是N存在2p轨道上的半充满状态,据此判断.
解答:
解:A、只含一种元素的物质不一定是纯净物,如氧气和臭氧的混合物中只含有一种元素,属于混合物,故A错误;
B、一个酸分子电离出n个氢离子,该酸为n元酸,含氧酸中含几个羟基氢原子则为几元酸,与分子中H原子数目无关,故B错误;
C、由同种元素组成的不同单质,互称为同素异形体,金刚石、石墨、C60互均是碳元素形成的不同单质,互为同素异形体,故C正确;
D、同周期元素从左到右元素的第一电离能逐渐增大,由于N2p轨道为半饱和状态,较为定,难以失去电子,则C、N、O三种元素第一电离能从大到小的顺序是N>O>C,故D错误.
故选C.
B、一个酸分子电离出n个氢离子,该酸为n元酸,含氧酸中含几个羟基氢原子则为几元酸,与分子中H原子数目无关,故B错误;
C、由同种元素组成的不同单质,互称为同素异形体,金刚石、石墨、C60互均是碳元素形成的不同单质,互为同素异形体,故C正确;
D、同周期元素从左到右元素的第一电离能逐渐增大,由于N2p轨道为半饱和状态,较为定,难以失去电子,则C、N、O三种元素第一电离能从大到小的顺序是N>O>C,故D错误.
故选C.
点评:本题主要考查的是纯净物、混合物的概念,同素异形体的定义等,难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
一定质量的铁铝合金完全溶于过量的稀硝酸中,反应过程中共产生4.48LNO(标准状况下测定),若在反应后的溶液中加入足量的氢氧化物溶液,则生成沉淀的质量不可能是( )
| A、21.4g | B、18.7g |
| C、15.6g | D、7.8g |
化学与生活密切相关,下列有关说法正确的是( )
| A、制作航天服的聚酯纤维属于新型无机非金属材料 |
| B、银器久置后表面变暗,是因为发生了电化学腐蚀 |
| C、Li是最轻的金属,也是活动性很强的金属,是制造电池的理想物质 |
| D、海水提取溴、煤的液化、焰色反应都发生了化学变化 |
 水系锂电池具有安全、环保和价格低廉等优点成为当前电池研究领域的热点.以钒酸钠(NaV3O8)为正极材料的电极反应式为:NaV3O8+xLi++xe-=NaLixV3O8,则下列说法不正确的是( )
水系锂电池具有安全、环保和价格低廉等优点成为当前电池研究领域的热点.以钒酸钠(NaV3O8)为正极材料的电极反应式为:NaV3O8+xLi++xe-=NaLixV3O8,则下列说法不正确的是( )| A、放电时,负极的电极反应式:Li-e-═Li+ |
| B、充电过程中Li+从阳极向阴极迁移 |
| C、充电过程中阳极的电极反应式为NaLixV3O8-xe-=NaV3O8+xLi+,NaLixV3O8中钒的化合价发生变化 |
| D、该电池可以用硫酸钠溶液作电解质 |
下列关于氨分子的化学用语错误的是( )
| A、化学式:NH3 |
B、电子式: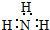 |
C、结构式: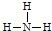 |
D、比例模型: |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、将1molCl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA | ||
| B、常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA | ||
| C、标准状况下,2.24L的CCl4中含有的C-Cl键数为0.4NA | ||
D、将CO2通过Na2O2使其增重a克时,反应中转移电子数为
|
 卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们. 为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置[已知:酸性H2SO3>H2CO3,Ca(HSO3)2溶于水]:
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置[已知:酸性H2SO3>H2CO3,Ca(HSO3)2溶于水]: