��Ŀ����
16���ҹ�������Ӧ���������칤������йء�������Ǧ���ļ��أ���¯��ʯ��̼��п��ʮ�װ����һ����ڣ������̣�����Ȼ�������ú̿����ʢ�������н�������Ѻ죬�����䶨�ٹ�ȡ������������ǦҲ������������Ǧ�����ͣ�����֮Ի�����������ѧ֪ʶ��������������жϣ����������ҹ���ʷ��Ǧ��ʹ������п��
��п��Ǧ�������Ե�п�����ã�
��Ǧ���طŵ�ʱ�������������������ӣ�
�ܡ�������Ǧ�������Ȼ�ԭ��ұ��������
| A�� | ��һ����ȷ | B�� | ��������ȷ | C�� | ��������ȷ | D�� | �ľ����ȷ |
���� ��Ŀ�漰��Ӧԭ��ΪZnCO3+2C$\frac{\underline{\;����\;}}{\;}$Zn+3CO�����ɽ������˳���֪п�Ļ����Ա�Ǧǿ���ϲ����ý���ʹ�ý��磬�Դ˽����⣮
��� �⣺��п�Ļ����Ա�Ǧǿ��Ǧ�����ұ����ʹ��ʱ���п�磬�ʢ���ȷ��
���ɽ������˳���֪п�Ļ����Ա�Ǧǿ���ʢ���ȷ��
��Ǧ�����ڷŵ�����У�����Pbת��Ϊ����Ǧ������Ǧ���������ᣬ�����ɵ�����Ǧ�����ڸ�����ʹ�������������ʢ���ȷ��
�ܡ�������Ǧ������̼�ڼ���������ұ�������������Ȼ�ԭ��ұ���������ʢ���ȷ��
��ѡD��
���� ���⿼�������ұ����Ϊ��Ƶ���㣬������Ԫ�ػ�����֪ʶ���ۺ���������õĿ��飬����ʱע����������Ϣ���ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
4������������ԭ��Ӧ�У�H2O�����������ǣ�������
| A�� | Cl2+H2O�THCl+HClO | B�� | 3Fe+4H2O��g��$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2 | ||
| C�� | 2Na2O2+2H2O�T4NaOH+O2�� | D�� | 2F2+2H2O�T4HF+O2 |
11��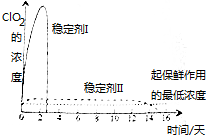 Ŀǰ���ȵ���������Cl2O��ClO2��Cl2O7�ȣ�����ClO2��Cl2���������������������ˮ�������߱��ʵȷ���Ӧ�ù㷺���й����ݼ��±���
Ŀǰ���ȵ���������Cl2O��ClO2��Cl2O7�ȣ�����ClO2��Cl2���������������������ˮ�������߱��ʵȷ���Ӧ�ù㷺���й����ݼ��±���
��ش��������⣺
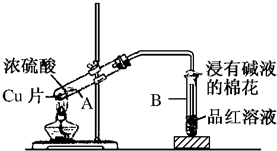
��1�����¡���ѹ�£������������������������Cl2O��ClO2��
��2��ClO2�ǵ��Ĵ���Ч�����Ĺ�����������������NaClO2��Һ��NCl3��Һ��Ӧ�Ƶã��䷴Ӧ�����ӷ���ʽΪNCl3+6ClO2-+3H2O�T6ClO2+3Cl-+3OH-+Y����Y�Ļ�ѧʽ��NH3��
��3��NaClO2�����������¿ɷ�����Ӧ����NaCl���ͷų�ClO2���÷�Ӧ�����ӷ���ʽ��4H++5ClO2-=Cl-+4ClO2��+2H2O��
��4��������ClO2���ȶ��Ԣ�͢�����ͷ�ClO2��Ũ����ʱ��ı仯��ͼ��ʾ������������ˮ�����ʣ�����ΪЧ���Ϻõ��ȶ������ȶ�������ԭ�����ȶ�������Ի����ͷ�ClO2���ܽϳ�ʱ��ά�ֱ��������Ũ�ȣ�
 Ŀǰ���ȵ���������Cl2O��ClO2��Cl2O7�ȣ�����ClO2��Cl2���������������������ˮ�������߱��ʵȷ���Ӧ�ù㷺���й����ݼ��±���
Ŀǰ���ȵ���������Cl2O��ClO2��Cl2O7�ȣ�����ClO2��Cl2���������������������ˮ�������߱��ʵȷ���Ӧ�ù㷺���й����ݼ��±���| ��ѧʽ | Cl2O | ClO2 | Cl2O7 |
| �е�/�� | 3.8 | 11.0 | 82.0 |
��1�����¡���ѹ�£������������������������Cl2O��ClO2��
��2��ClO2�ǵ��Ĵ���Ч�����Ĺ�����������������NaClO2��Һ��NCl3��Һ��Ӧ�Ƶã��䷴Ӧ�����ӷ���ʽΪNCl3+6ClO2-+3H2O�T6ClO2+3Cl-+3OH-+Y����Y�Ļ�ѧʽ��NH3��
��3��NaClO2�����������¿ɷ�����Ӧ����NaCl���ͷų�ClO2���÷�Ӧ�����ӷ���ʽ��4H++5ClO2-=Cl-+4ClO2��+2H2O��
��4��������ClO2���ȶ��Ԣ�͢�����ͷ�ClO2��Ũ����ʱ��ı仯��ͼ��ʾ������������ˮ�����ʣ�����ΪЧ���Ϻõ��ȶ������ȶ�������ԭ�����ȶ�������Ի����ͷ�ClO2���ܽϳ�ʱ��ά�ֱ��������Ũ�ȣ�
1�����ܱ�������A��B��Ӧ����C���䷴Ӧ���ʷֱ���v��A����v��B����v��C����ʾ����֪v��A����v��B����v��C��֮�������¹�ϵ��3v��B��=2v��A����2v��B��=3v��C������˷�Ӧ�ɱ�ʾΪ��������
| A�� | 3A+B=C | B�� | 2A+2B=3C | C�� | 4A+6B=9C | D�� | 9A+6B=4C |
8���������ʼӹ���Ӧ����δ�����仯ѧ���ʵ��ǣ�������
| ѡ�� | A | B | C | D |
| �ӹ���Ӧ�� |  ��֬��Ӳ�� |  ������� |  ʯӢ������ź� |  Ư������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
6�������й�˵����ȷ���ǣ�������
| A�� | 1 mol FeBr2������������Ӧʱ��������ת�Ƶĵ�����ԼΪ3��6.02��1023 | |
| B�� | �����£�pH��Ϊ3��������Һ����HCl��Һ ��H2SO4��Һ��CH3COOH��Һ���������ʵ����ʵ���Ũ�ȴ�С˳��Ϊ��=�ڣ��� | |
| C�� | �������NaCl��AlCl3��ȡNa��Al | |
| D�� | һ�������·�ӦCr2O72-��aq��+H2O��l��?2CrO42-��aq��+2H+��aq���ﵽƽ��μ�����Ũ���ᣬ���´�ƽ��ǰ��2v����Cr2O72-����v����CrO42-�� |
 ����CH2=CH2��
����CH2=CH2�� ����CH��CH��CH3-C��CH����CH3-Cl����CH3-CH2-Br��CH3-OH����CH3-CH2-OH⑪CH3-COOH⑫CH3-COO-CH2-CH3⑬
����CH��CH��CH3-C��CH����CH3-Cl����CH3-CH2-Br��CH3-OH����CH3-CH2-OH⑪CH3-COOH⑫CH3-COO-CH2-CH3⑬ ⑭
⑭ ⑮
⑮ ⑯
⑯
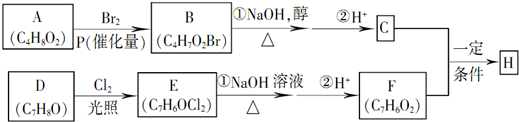
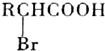
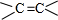 ��
��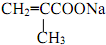 +NaBr+2H2O���÷�Ӧ������Ϊ��ȥ��Ӧ��
+NaBr+2H2O���÷�Ӧ������Ϊ��ȥ��Ӧ�� $\stackrel{һ������}{��}$
$\stackrel{һ������}{��}$ +H2O��
+H2O��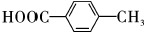 ��
��