题目内容
15.下列有关试剂的保存方法,错误的是( )| A. | 金属钠保存在煤油中 | |
| B. | 存放FeSO4溶液时加入少量铁粉 | |
| C. | NaOH溶液保存在带胶塞的玻璃试剂瓶中 | |
| D. | 浓硝酸保存在无色细口瓶中 |
分析 A、金属钠和煤油不反应,且密度比煤油大;
B、FeSO4溶液容易被氧气氧化;
C、NaOH能和玻璃反应生成硅酸钠;
D、浓硝酸见光易分解.
解答 解:A、金属钠和煤油不反应,且密度比煤油大,故保存在煤油中能隔绝空气隔绝水,故A正确;
B、FeSO4溶液容易被氧气氧化,故加入铁粉可以将生成的铁离子还原为亚铁离子,故B正确;
C、NaOH能和玻璃反应生成硅酸钠,故不能如果储存在玻璃瓶中则应用橡胶塞,故C正确;
D、浓硝酸见光易分解,故应保存在棕色试剂瓶中,且避光保存,故D错误.
故选D.
点评 本题考查了常见试剂的存放,难度不大,应注意的是氢氧化钠溶液如果存放在玻璃瓶中的话,应用橡胶塞.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
6.玻璃、水泥、陶瓷属于( )
| A. | 金属材料 | B. | 无机非金属材料 | C. | 有机高分子材料 |
10.下列各组数据关系中,前者比后者大的是( )
| A. | 纯水100℃和25℃的pH值 | |
| B. | Na2CO3溶液中2c(CO32-)和c(Na+) | |
| C. | 100mL 0.1mol/L的CH3COOH溶液与10mL 1.0mol/L的CH3COOH溶液中H+数目 | |
| D. | 同温下pH=11的KOH与pH=3的CH3COOH溶液中由水电离出的OH-离子浓度 |
20.在2A+B?3C+4D反应中,表示该反应速率最快的是( )
| A. | v(D)=1mol/(L•s) | B. | v(B)=1mol/(L•min) | C. | v(A)=0.5mol/(L•s) | D. | v(C)=0.8mol/(L•s) |
7.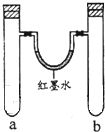 某化学小组用以下装置做兴趣实验(试管中有空气存在).
某化学小组用以下装置做兴趣实验(试管中有空气存在).
(1)实验1,同时加入试剂,反应开始可观察到U形管中液面b(填编号),简述产生该现象的原因钠与水反应比钠与乙醇反应快,所以开始时a试管中产生的氢气比b试管多,故液面应左低右高.
a.左高右低b.左低右高c.左右相平d.来回震荡
(2)写出钠与乙醇反应的化学方程式2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;反应结束静置一段时间,最终U形管中液面c(填题(1)编号).
(3)实验2,U形管中液面a(填题(1)编号);写出a试管中发生还原反应的电极反应方程式O2+2H2O+4e→4OH-.
(4)实验3,U形管中液面左低右高,检验b管中生成新物质的操作是取样,加入KSCN溶液,溶液变红,说明有Fe3+生成.
(5)其他条件不变情况下,将实验4a、b试管中硝酸同时改为3mLcd(填编号),即可观察到U形管液面产生相反现象.
a.无水乙醇b.浓硫酸c.稀硫酸d.浓盐酸
(6)常温下,在a、b试管中分别加入等体积的同种溶液,仅对a试管进行强光照射,一段时间后观察到U型管液面左低右高,根据所学知识,推测该溶液为氯水(写名称).
 某化学小组用以下装置做兴趣实验(试管中有空气存在).
某化学小组用以下装置做兴趣实验(试管中有空气存在).| 实验编号 | a中试剂 | b中试剂 |
| 1 | 0.1克Na、3mL水 | 0.1克Na、3mL乙醇 |
| 2 | 铁钉、3mL饱和食盐水 | 铁钉、3mL饱和氯化铵 |
| 3 | 3mL水 | 3mL饱和FeSO4溶液 |
| 4 | 3mL浓硝酸、1g铝片 | 3mL浓硝酸、1g铜片 |
a.左高右低b.左低右高c.左右相平d.来回震荡
(2)写出钠与乙醇反应的化学方程式2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;反应结束静置一段时间,最终U形管中液面c(填题(1)编号).
(3)实验2,U形管中液面a(填题(1)编号);写出a试管中发生还原反应的电极反应方程式O2+2H2O+4e→4OH-.
(4)实验3,U形管中液面左低右高,检验b管中生成新物质的操作是取样,加入KSCN溶液,溶液变红,说明有Fe3+生成.
(5)其他条件不变情况下,将实验4a、b试管中硝酸同时改为3mLcd(填编号),即可观察到U形管液面产生相反现象.
a.无水乙醇b.浓硫酸c.稀硫酸d.浓盐酸
(6)常温下,在a、b试管中分别加入等体积的同种溶液,仅对a试管进行强光照射,一段时间后观察到U型管液面左低右高,根据所学知识,推测该溶液为氯水(写名称).
4.下列说法正确的是( )
| A. | CaCl2晶体中的只含离子键 | |
| B. | 某物质在熔融态能导电,则该物质中一定含有离子键 | |
| C. | N2和HCl两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| D. | 干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力 |

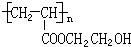 .
.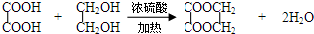 .
.
