题目内容
5.有以下几种物质①熔融氯化钠 ②浓硫酸 ③Cu ④蔗糖 ⑤CH3COOH ⑥NaHCO3 ⑦酒精 ⑧液溴,填空回答:(填序号)(1)以上物质中属于强电解质的是①⑥; 属于非电解质的是④⑦.
(2)写出⑤在水中的电离反应方程式:CH3COOH?CH3COO-+H+.
分析 (1)电解质是指:在水溶液中或熔融状态下能够导电的化合物;强电解质是在水溶液中或熔融状态下,能完全电离的电解质;包括强酸、强碱、活泼金属氧化物和大部分盐;弱电解质是在水溶液中不能完全电离的电解质,包括弱酸、弱碱、水等;非电解质是指:在熔融状态和水溶液中都不能导电的化合物,非电解质在熔融状态和水溶液中自身都不能离解出自由移动的离子;
(2)⑤CH3COOH 为弱酸在溶液中部分电离.
解答 解:(1)①熔融氯化钠能完全电离出钠离子和氯离子,为化合物,属于强电解质;
②浓硫酸为硫酸的浓溶液为混合物,既不是电解质,也不是非电解质;
③Cu为单质,既不是电解质,也不是非电解质;
④蔗糖在熔融状态和水溶液中都只存在蔗糖分子,不能导电,为非电解质;
⑤CH3COOH在水溶液中部分电离:CH3COOH?CH3COO-+H+属于弱电解质;
⑥NaHCO3在水溶液中或熔融状态下能够完全电离,电离方程式为:NaHCO3═Na++HCO3-,属于强电解质;
⑦酒精水溶液中都只存在乙醇分子,不能导电,为非电解质;
⑧液溴为单质,既不是电解质,也不是非电解质;
故答案为:①⑥;④⑦;
(2)⑤CH3COOH 为弱酸在溶液中部分电离,电离出乙酸根离子和氢离子,电离方程式为:CH3COOH?CH3COO-+H+,
故答案为:CH3COOH?CH3COO-+H+;
点评 本题考查了电解质与非电解质、强弱电解质的定义,侧重考查学生的辨别能力,注意明确电解质与非电解质的区别,单质和混合物既不是电解质,也不是非电解质,题目难度不大.

练习册系列答案
相关题目
7.下列说法中,正确的是( )
| A. | 制取水泥和玻璃的原料中都含有石灰石 | |
| B. | 普通玻璃是电的绝缘体,这种透明的固体物质属于晶体 | |
| C. | 石英玻璃能经受温度剧变且抵抗酸碱的腐蚀 | |
| D. | 硅酸盐可用氧化物表示其组成,这表明硅酸盐是由氧化物组成的 |
11.根据如图判断,下列说法正确的是( )
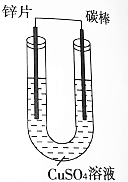

| A. | 该过程化学能转化为热能 | |
| B. | 该反应过程中只有化学键形成,没有化学键断裂 | |
| C. | CuSO4溶液里Cu2+移向负极 | |
| D. | 可以用铜片代替碳棒 |
17.下列各组中的反应,属于同一反应类型的是( )
| A. | 由溴乙烷制乙醇;由乙烯与水反应制乙醇 | |
| B. | 乙烯使溴的CCl4溶液褪色;甲苯使酸性高锰酸钾溶液褪色 | |
| C. | 由苯制硝基苯;由环己醇制环己烯 | |
| D. | 由乙酸和乙醇制乙酸乙酯;苯与液溴在FeBr3催化下制溴苯 |
14.某物质加入到溴水中振荡混合,静置后分为两层,上层几乎呈无色,该物质是( )
| A. | 酒精溶液 | B. | 四氯化碳 | C. | 碘化钾溶液 | D. | 食盐水 |
15.下列有关试剂的保存方法,错误的是( )
| A. | 金属钠保存在煤油中 | |
| B. | 存放FeSO4溶液时加入少量铁粉 | |
| C. | NaOH溶液保存在带胶塞的玻璃试剂瓶中 | |
| D. | 浓硝酸保存在无色细口瓶中 |
 +H+=
+H+=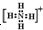 ;由5个原子核10个电子组成的化合物电子式是
;由5个原子核10个电子组成的化合物电子式是 ,结构式是
,结构式是 .
.