题目内容
在一定条件下,化学平衡 2HI(g)?H2(g)+I2(g)(正反应为吸热反应):
(1)如果升高温度,平衡混合物的颜色 ;
(2)如果加入一定量的H2,平衡 移动;
(3)如果是密闭容器的体积增大,平衡 移动.
(1)如果升高温度,平衡混合物的颜色
(2)如果加入一定量的H2,平衡
(3)如果是密闭容器的体积增大,平衡
考点:化学平衡的影响因素
专题:化学平衡专题
分析:(1)升高温度化学平衡向着吸热方向进行;
(2)增大生应物浓度,平衡逆向移动;
(3)减小压强,平衡向着气体体积增大的方向移动.
(2)增大生应物浓度,平衡逆向移动;
(3)减小压强,平衡向着气体体积增大的方向移动.
解答:
解:2HI(g)?H2(g)+I2(g)(正反应为吸热反应)
(1)升高温度化学平衡向着吸热方向进行,故平衡正向移动,颜色变深,
故答案为:变深;
(2)增大生应物浓度,平衡逆向移动,
故答案为:向左;
(3)该反应反应前后气体的体积不变,故减小压强,平衡不移动,
故答案为:不.
(1)升高温度化学平衡向着吸热方向进行,故平衡正向移动,颜色变深,
故答案为:变深;
(2)增大生应物浓度,平衡逆向移动,
故答案为:向左;
(3)该反应反应前后气体的体积不变,故减小压强,平衡不移动,
故答案为:不.
点评:本题考查影响化学平衡移动的因素,难度不大.要熟练掌握勒夏特列原理.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
硝酸汞和碘化钾溶液混合后会生成红色的碘化汞沉淀,为了探究硝酸汞和碘化钾溶液之间能否发生氧化还原反应,研究人员设计了如图的实验装置,结果电流计指针发生了偏转,下列分析正确的是( )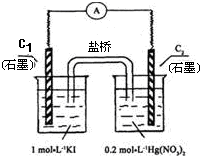

| A、C1电极上发生的反应是:2I--2e-=I2 |
| B、如图装置的电流方向是从C1到C2 |
| C、盐桥中的K+离子向C1电极移动 |
| D、装置发生的总反应是Hg2++2I-=HgI2↓ |
化学在生活中无处不在,其中不科学的是( )
| A、含食品添加剂的食品都不属于绿色食品 |
| B、维生素C具有还原性,在人体内起抗氧化作用 |
| C、为防止月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁 |
| D、地震后防疫人员在震区周围撒石灰,其作用是进行环境消毒,防止灾后出现疫情 |
可逆反应aA(?)+2B(g)?2C(g)+D(g),其中a为正整数.反应中当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )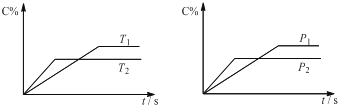

| A、达到平衡后,加入催化剂则C%增大 |
| B、达到平衡后,若升高温度,平衡正向移动 |
| C、a可以为任意的正整数 |
| D、达平衡后,增加A的量,有利于平衡正向移动 |
相同质量的两份铝,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气的物质的量之比为( )
| A、1:1 | B、1:6 |
| C、2:3 | D、3:2 |
 某研究性学习小组的课题为“Mg、C原电池电解淀粉KI溶液的研究”,其研究装置如图所示.下列有关说法不正确的是( )
某研究性学习小组的课题为“Mg、C原电池电解淀粉KI溶液的研究”,其研究装置如图所示.下列有关说法不正确的是( )| A、镁为负极,发生氧化反应 |
| B、原电池中碳极反应式为Fe3++e-═Fe2+ |
| C、电解池中阴极处变蓝 |
| D、电解池中阴极处变红 |
等质量的铝分别与足量的稀盐酸和氢氧化钠溶液反应,当铝完全溶解时,反应中消耗的HCl和NaOH物质的量之比为( )
| A、1:1 | B、2:1 |
| C、1:2 | D、3:1 |
下列各组物质熔点由低到高排列的是( )
| A、H2O、H2S、H2Se、H2Te |
| B、F2、Cl2、Br2、I2 |
| C、Li、Na、K、Rb |
| D、干冰、MgCl2、金刚石、晶体硅 |