题目内容
18.某地方政府为了实现对当地水资源及沿途流域环境的综合治理,引导甲、乙两个相邻的工厂在污水处理方面做了横向联合.已知两厂排放的污水经初步处理后,分别只有下列8种离子中的4种(两厂不含相同离子):Ag+、Ba2+、Fe3+、Na+、Cl-、SO42-、NO3-、OH-.两厂单独排放都会造成严重的水污染,如将两厂的污水按一定的比例混合,沉淀后污水便变成无色澄清的溶液而排放,污染程度会大大降低.关于污染源的分析,你认为正确的是( )| A. | SO4-和NO3-可能来自同一工厂 | B. | Cl-和NO3-一定来自不同的工厂 | ||
| C. | Ag+和Na+可能来自同一工厂 | D. | Na+和NO3-来自同一工厂 |
分析 Ag+、Fe3+均OH-结合生成沉淀,不能共存,SO42-与Ba2+结合生成沉淀,Ag+、Cl-结合生成沉淀,不能共存,结合各含4种离子来解答.
解答 解:Ag+、Fe3+均OH-结合生成沉淀,SO42-与Ba2+结合生成沉淀,Ag+、Cl-结合生成沉淀,不能共存,
则一个厂含Ba2+、Ag+、Fe3+、NO3-,
另一个厂含Na+、Cl-、SO42-、OH-,
将两厂的污水按一定的比例混合,沉淀后污水便变成无色澄清的溶液而排放,污染程度会大大降低,
显然只有B合理,
故选B.
点评 本题考查常见离子的检验,为高频考点,把握离子之间的反应、离子共存为解答关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
相关题目
8.科学研究、工业生产和日常生活都离不开物质的制备.
(一)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)?4NO2(g)+O2(g)△H>0
(1)反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将不变填(“增大”、“减小”或“不变”).
(2)下表为反应在T1温度下的部分实验数据:
则500s内N2O5的分解速率为3.00×10-3mol/(L.S).
(3)在T2温度下,反应1000s时测得N2O5的浓度为3.00mol/L,则T2<T1(填“>“、“<”或“=”).
(二)工业上用重晶石(主要成分为BaSO4)制备BaCl2
(1)BaSO4与碳在高温下反应生成一氧化碳与金属硫化物,该反应中每1mol碳生成CO需要吸收142.8kJ的热量,此反应的热化学方程式为BaSO4(s)+4C(s)═4CO(g)+BaS(s)△H=+571.2kJ/mol.
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,$\frac{c(B{r}^{-})}{c(C{l}^{-})}$=2.7×10-3.(Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10)
(3)若NaOH溶液吸收H2S气体生成等物质的量的Na2S和NaHS,则溶液中各离子浓度由大到小的顺序为c(Na+)>c(HS-)>c(S2-)>c(OH-)>c(H+).
(一)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)?4NO2(g)+O2(g)△H>0
(1)反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将不变填(“增大”、“减小”或“不变”).
(2)下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5/mol/L) | 5.00 | 3.50 | 2.50 |
(3)在T2温度下,反应1000s时测得N2O5的浓度为3.00mol/L,则T2<T1(填“>“、“<”或“=”).
(二)工业上用重晶石(主要成分为BaSO4)制备BaCl2
(1)BaSO4与碳在高温下反应生成一氧化碳与金属硫化物,该反应中每1mol碳生成CO需要吸收142.8kJ的热量,此反应的热化学方程式为BaSO4(s)+4C(s)═4CO(g)+BaS(s)△H=+571.2kJ/mol.
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,$\frac{c(B{r}^{-})}{c(C{l}^{-})}$=2.7×10-3.(Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10)
(3)若NaOH溶液吸收H2S气体生成等物质的量的Na2S和NaHS,则溶液中各离子浓度由大到小的顺序为c(Na+)>c(HS-)>c(S2-)>c(OH-)>c(H+).
6.有关油脂的说法,错误的是( )
| A. | 油脂是人体不可缺少的营养物质 | |
| B. | 油脂的水解产物是氨基酸 | |
| C. | 油脂主要在小肠中被消化吸收 | |
| D. | 脂肪中多不饱和酸含量越高,其营养价值也越高 |
3.利用如图所示装置,将10mL CCl4(沸点76.7℃)和10mL甲苯(沸点110.6℃)的混合物进行蒸馏分离.下列说法正确的是( )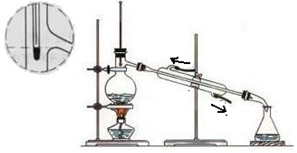

| A. | 冷凝水的进出口方向正确 | B. | 应选用20 mL的蒸馏烧瓶 | ||
| C. | 温度计液泡应插在混合液中 | D. | 锥形瓶中收集到的是甲苯 |
7.2009年9月25日,我国成功发射“神舟七号”载人飞船.飞船以铝粉与高氯酸铵的混合物为固体燃料,其中高氯酸铵的反应为:2NH4ClO4═N2↑+Cl2↑+2O2↑+4H2O.下列有关叙述正确的是( )
| A. | 铝粉的作用是点燃时可以置换出氧气 | |
| B. | 在反应中NH4ClO4仅起到氧化剂作用 | |
| C. | 该反应属于分解反应,也属于氧化还原反应 | |
| D. | 上述反应瞬间能产生高温,高温是推动飞船飞行的主要因素 |
8.下列关于物质的用途说法不正确的是( )
| A. | 过氧化钠可以用呼吸面具中供氧剂 | |
| B. | 氧化铝的熔点高,可用作耐火材料 | |
| C. | 铝热反应原理是炼铁最常见的反应原理 | |
| D. | 青铜是我国使用最早的合金 |