题目内容
9.燃烧a g乙醇(液态)生成CO2气体和液态H2O,放出热量为QkJ,经测定ag乙醇与足量Na反应能生成H25.6L(标准状况下),则表示乙醇燃烧热的热化学方程式为C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-2QkJ/mol(△H的值不用a表示)分析 由a g乙醇与足量钠反应,能生成标准状况下的氢气5.6L,根据氢气的量可求出a g乙醇的物质的量.由于燃烧a g乙醇(液),生成二氧化碳气体和液态水,放出的热量为QkJ,然后求出1mol乙醇生成二氧化碳气体和液态水,放出的热量,据此写出热化学反应方程式.
解答 解:a g乙醇与足量钠反应,能生成标准状况下的氢气5.6L,生成氢气的物质的量为:$\frac{5.6L}{22.4L/mol}$=0.25mol,
由关系式2C2H5OH~H2可知,a g乙醇的物质的量为0.5mol,
由于燃烧a g乙醇(液)生成二氧化碳气体和液态水,放出的热量为QkJ,即燃烧0.5mol乙醇(液),生成二氧化碳气体和液态水,放出的热量为QkJ,则燃烧1mol乙醇时放出热量为2QkJ,
所以该条件下乙醇燃烧的热化学方程式为:C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-2QkJ/mol,
故答案为:C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-2QkJ/mol.
点评 本题考查热化学反应方程式的书写,难度不大,根据氢气的体积计算出乙醇的物质的量为解答关键,注意掌握热化学方程式的书写原则,试题有利于培养学生的分析能力及化学计算能力.

练习册系列答案
相关题目
13.能够使醋酸溶液的c(H+)减小和醋酸的电离平衡逆向移动的条件是( )
| A. | 滴加少量H2SO4溶液 | B. | 加入少许水稀释 | ||
| C. | 滴加少量NaOH溶液 | D. | 加入少许CH3COONa晶体 |
14.实验室进行下列实验时,一定不需要使用“沸石”的是( )
| A. | 制取蒸馏水 | B. | 分馏石油 | C. | 制取乙烯 | D. | 溴乙烷的水解 |
11.120℃、101kPa时,两种气态烃的混合物2L完全燃烧,得到相同状况下3L CO2和3L水蒸气.这两种烃的可能组成是( )
| A. | CH4和C2H4 | B. | C2H6和C2H2 | C. | C3H8和C2H4 | D. | CH4和C2H2 |
4. 2013年12月2日嫦娥三号探测器由长征三号乙运载火箭从西昌卫星发射中心发射,首次实现月球软着陆和月面巡视勘察.长征三号乙运载火箭用的燃料是液态偏二甲基肼C2H8N2,氧化剂是液态N2O4,已知1.5g偏二甲基肼完全燃烧生成液态水放出50kJ热量,则下列热化学方程式正确的是( )
2013年12月2日嫦娥三号探测器由长征三号乙运载火箭从西昌卫星发射中心发射,首次实现月球软着陆和月面巡视勘察.长征三号乙运载火箭用的燃料是液态偏二甲基肼C2H8N2,氧化剂是液态N2O4,已知1.5g偏二甲基肼完全燃烧生成液态水放出50kJ热量,则下列热化学方程式正确的是( )
 2013年12月2日嫦娥三号探测器由长征三号乙运载火箭从西昌卫星发射中心发射,首次实现月球软着陆和月面巡视勘察.长征三号乙运载火箭用的燃料是液态偏二甲基肼C2H8N2,氧化剂是液态N2O4,已知1.5g偏二甲基肼完全燃烧生成液态水放出50kJ热量,则下列热化学方程式正确的是( )
2013年12月2日嫦娥三号探测器由长征三号乙运载火箭从西昌卫星发射中心发射,首次实现月球软着陆和月面巡视勘察.长征三号乙运载火箭用的燃料是液态偏二甲基肼C2H8N2,氧化剂是液态N2O4,已知1.5g偏二甲基肼完全燃烧生成液态水放出50kJ热量,则下列热化学方程式正确的是( )| A. | C2H8N2(l)+2N2O4(l)═3N2(g)+2CO2(g)+4H2O(l)△H=-50kJ•mol-1 | |
| B. | C2H8N2(l)+2N2O4(l)═3N2(g)+2CO2(g)+4H2O(g)△H=-50kJ•mol-1 | |
| C. | C2H8N2(l)+2N2O4(l)═3N2(g)+2CO2(g)+4H2O(l)△H=-2000kJ•mol-1 | |
| D. | C2H8N2(l)+2N2O4(l)═3N2(g)+2CO2(g)+4H2O(g)△H=-2000kJ•mol-1 |
14.某学生设计如图实验步骤测定铁铜合金的组成:
说明:以上所有气体体积都已换算成标准状况时的数据
下列说法正确的是( )

说明:以上所有气体体积都已换算成标准状况时的数据
下列说法正确的是( )
| A. | 不溶物Y为Cu且质量是1.6g | |
| B. | 合金中铁单质的质量是1.68g | |
| C. | 合金中氧元素的物质的量是0.01mol | |
| D. | X溶液中既含有CuSO4又含有FeSO4 |
1.下列各组物质中,既不是同系物,又不是同分异构体的是( )
| A. | 苯甲酸和 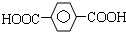 | B. | 乙酸和2-甲基丙酸 | ||
| C. | 硝基乙烷和氨基乙酸 | D. | 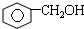 和 和 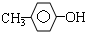 |
18.下列离子方程式正确的是( )
| A. | Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+=2Fe3++3H2O | |
| B. | 氯化铝溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ | |
| C. | FeBr2溶液中加入过量的氯水:2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| D. | 铝和烧碱溶液:2Al+2OH-+2H2O=2AlO2-+3H2↑ |