题目内容
13.能够使醋酸溶液的c(H+)减小和醋酸的电离平衡逆向移动的条件是( )| A. | 滴加少量H2SO4溶液 | B. | 加入少许水稀释 | ||
| C. | 滴加少量NaOH溶液 | D. | 加入少许CH3COONa晶体 |
分析 向醋酸溶液中加入含有CH3COO-或H+的物质能抑制醋酸电离,电离平衡向左移动,若使c(H+)减小,可以加入醋酸根离子,据此分析解答.
解答 解:A、加入硫酸,氢离子浓度增大,故A错误;
B、加水稀释促进醋酸电离,故B错误;
C、加入NaOH溶液,醋酸电离平衡正向移动,故C错误;
D、加入醋酸根离子,抑制醋酸电离且氢离子浓度减小,故D正确;
故选D.
点评 本题考查了影响弱电解质电离的因素,难度不大,注意:如果加入含有相同离子的物质就抑制其电离,如果加入和弱电解质电离的离子发生反应的物质就促进其电离.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
3.下列物质中俗称为纯碱的是( )
| A. | NaHCO3 | B. | NaOH | C. | Na2CO3 |
4.你认为下列数据可信的是( )
| A. | 用广泛pH试纸测得某盐酸溶液的pH是3.2 | |
| B. | 某常见气体的密度为1.8g/cm3 | |
| C. | 某澄清石灰水的浓度为2mol/L | |
| D. | 某元素的原子半径是0.160nm |
1.下列说法不正确的是( )
| A. | 第二周期元素从C到F,非金属性逐渐减弱 | |
| B. | 第三周期元素从Na到Cl,原子半径逐渐增大 | |
| C. | HF、HCl、HBr、HI的热稳定性依次减弱 | |
| D. | LiOH、NaOH、KOH的碱性依次增强 |
8.假设某化学反应的反应过程如下图所示观察分析,符合图中变化的化学反应为( )


| A. | A2+3B2?2AB3 | B. | 2AB2+B2?2AB3 | C. | 2A2 B+5B2═4AB3 | D. | 2AB2+B2═2AB |
5.下列化合物的核磁共振氢谱中出现两组峰且峰面积之比是2:1的是( )
| A. | 乙酸甲酯 | B. | 对苯二酚 | C. | 2--甲基丙烷 | D. | 对二甲苯 |
 已知A是一种相对分子质量为28的气态烃,它可转化为其他常见有机物,转化关系如图所示.
已知A是一种相对分子质量为28的气态烃,它可转化为其他常见有机物,转化关系如图所示.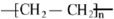 .
.