题目内容
18.下列离子方程式正确的是( )| A. | Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+=2Fe3++3H2O | |
| B. | 氯化铝溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ | |
| C. | FeBr2溶液中加入过量的氯水:2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| D. | 铝和烧碱溶液:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
分析 A.三价铁离子能够氧化碘离子生成单质碘;
B.一水合氨为弱碱,保留化学式;
C.氯水过量,二价铁离子、溴离子全部被氧化;
D.二者反应生成偏铝酸钠和氢气.
解答 解:A.Fe2O3溶于过量的氢碘酸中,离子方程式;Fe2O3+6H++2I-=2Fe2++I2+3H2O,故A错误;
B.氯化铝溶液中加入足量的氨水,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C.FeBr2溶液中加入过量的氯水,离子方程式:2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-,故C错误;
D.铝和烧碱溶液,离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑,故D正确;
故选:D.
点评 本题考查了离子方程式书写,侧重考查复分解反应、氧化还原反应的离子方程式书写,明确发生反应实质是解题关键,注意反应物用量对反应的影响,选项C为易错选项.

练习册系列答案
相关题目
3.下列关于${\;}_{2}^{3}$He的说法正确的是( )
| A. | ${\;}_{2}^{3}$He原子核内含有2个中子 | |
| B. | ${\;}_{2}^{3}$He原子核内含有2个质子 | |
| C. | ${\;}_{2}^{3}$He原子核外有3个电子 | |
| D. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He是两种不同的元素 |
10.反应4A(g)+3B(g)═2C(g)+D(g),经2min,B的浓度减少了0.6mol/L.下列反应速率的表示正确的是( )
| A. | 用A表示的反应速率是0.4 mol/(L•min) | |
| B. | 用C表示的反应速率是0.2 mol/(L•s) | |
| C. | 2 min末的反应速率,用B表示是0.3 mol/(L•min) | |
| D. | 2 min内,用B和C表示的反应速率之比为2:3 |
7.已知铝也能和氢氧化钠溶液反应:2Al+2NaOH+2H2O→2NaAlO2+3H2↑,现有两份铝,一份与过量的氢氧化钠溶液反应,另一份与过量的盐酸反应,若要制取等质量的氢气,则两份铝的质量比为( )
| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
8.下列离子方程式表达正确的是( )
| A. | 向硫酸铵溶液中滴加氢氧化钡溶液:Ba2++SO42-=BaSO4↓ | |
| B. | 钠跟水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | AlCl3溶液中加入过量氨水:Al3++4NH3.H2O=AlO2-+4NH4++2H2O | |
| D. | 用NaOH溶液吸收少量Cl2:Cl2+2OH-=Cl-+ClO-+H2O |
 .
. .
.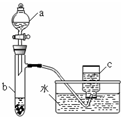 甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答.
甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答.