题目内容
4.在指定环境中,下列各组离子一定可以大量共存的是( )| A. | 使pH试纸呈红色的溶液中:I-、NO3-、SO42-、Na+ | |
| B. | 水电离出的c(H+)=1×10-13mol/L的溶液中:CO32-、K+、ClO-、SO32- | |
| C. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1012的溶液中:NH4+、Ca2+、C1-、K+ | |
| D. | 加入铝粉能产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- |
分析 A.使pH试纸呈红色的溶液呈酸性,硝酸根离子在酸性条件下能够氧化碘离子;
B.水电离出的c(H+)=1×10-13mol/L的溶液中存在大量氢离子或氢氧根离子,次氯酸根离子能够氧化亚硫酸根离子,亚硫酸根离子、碳酸根离子、次氯酸根离子与氢离子反应;
C.在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1012的溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应;
D.加入铝粉能产生大量氢气的溶液中存在大量氢离子或氢氧根离子,铵根离子与氢氧根离子反应.
解答 解:A.使pH试纸呈红色的溶液呈酸性,I-、NO3-在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.水电离出的c(H+)=1×10-13mol/L的溶液呈酸性或碱性,CO32-、ClO-、SO32-都与酸性溶液中的氢离子反应,ClO-、SO32-之间发生氧化还原反应,在溶液中一定不能大量共存,故B错误;
C.在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1012的溶液呈酸性,溶液中存在大量氢离子,NH4+、Ca2+、C1-、K+之间不发生反应,都不与氢离子反应,在溶液中能够大量共存,故C正确;
D.加入铝粉能产生大量氢气的溶液呈酸性或碱性,NH4+与碱性溶液中的氢氧根离子反应,在碱性溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

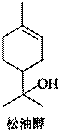 松油醇是一种天然有机化合物,存在于芳樟油、玉树油及橙花油等天然植物精油中,具有紫丁香香气,在香料工业中用途广泛,主要用于香皂及化妆品香料和调和香精.松油醇结构如下所示,下列有关松油醇的叙述错误的是( )
松油醇是一种天然有机化合物,存在于芳樟油、玉树油及橙花油等天然植物精油中,具有紫丁香香气,在香料工业中用途广泛,主要用于香皂及化妆品香料和调和香精.松油醇结构如下所示,下列有关松油醇的叙述错误的是( )| A. | 松油醇的分子式为C10H18O | |
| B. | 松油醇能发生加成反应、消去反应、氧化反应、酯化反应 | |
| C. | 松油醇存在酚类的同分异构体,分子中有2个手性碳原子 | |
| D. | 松油醇分子在核磁共振氢谱中有9个吸收峰 |
| A. | 该元素属于第6周期 | |
| B. | 该元素位于IVA族 | |
| C. | 该元素为金属元素,性质与82Pb(铅)相似 | |
| D. | 该元素原子含有114个电子和184个中子 |
| A. | NH3易液化,液氨常作制冷剂 | |
| B. | NO、NO2都是有毒气体 | |
| C. | 铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处 | |
| D. | 稀HNO3和活泼金属反应时主要得到氢气 |
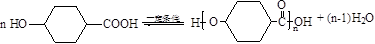 .
.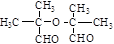 .
.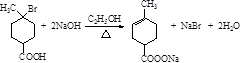 .
.