题目内容
10.我国古代科技在造纸、印刷、纺织、陶瓷、冶铸、火药等方面都有引以为傲的发明创造.下列说法正确的是( )| A. | 陶瓷的主要成分属于硅酸盐,硅酸盐与酸、碱都不反应 | |
| B. | 青铜铸造的器皿在空气中易发生析氢腐蚀,铜为原电池负极反应物 | |
| C. | 以树皮和麻绳为原料所造的纸张其主要成分是纤维素,纤维素与淀粉互为同分异构体 | |
| D. | 黑火药反应:2KNO3+S+3C═K2S+N2+3CO2 的还原剂只有C |
分析 A.有些硅酸盐与酸要反应,如硅酸钠与盐酸反应生成硅酸和氯化钠;
B.青铜为铜的合金,在空气中发生吸氧腐蚀;
C.分子式相同结构不同的有机物互为同分异构体;
D.含元素化合价升高的物质为还原剂,在反应中被氧化,以此来解答.
解答 解:A.有些硅酸盐与酸要反应,如硅酸钠与盐酸反应生成硅酸和氯化钠,故A错误;
B.青铜为铜的合金,铜不能与氢离子反应,在空气中氧气得电子,发生吸氧腐蚀,故B错误;
C.淀粉和纤维素的表达式虽然相同,但是聚合度n值不同,故分子式不同,二者不互为同分异构体,故C错误;
D.S+2KNO3+3C=K2S+N2↑+3CO2↑中,S、N元素的化合价降低,C元素化合价升高,只有C为还原剂,故D正确;
故选D.
点评 本题考查了常见物质的性质、氧还原反应中还原剂的判断、原电池原理质,熟悉相关物质的性质是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.高锰酸钾是中学化学常用的强氧化剂,实验室中可通过以下反应制得:
MnO2熔融氧化:3MnO2+KClO3+6KOH$\frac{\underline{\;熔化\;}}{\;}$3K2MnO4+KCl+3H2O
K2MnO4歧化:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
相关物质的溶解度数据见下表:
已知K2MnO4溶液显绿色,KMnO4溶液显紫红色.实验流程如下:
请回答:
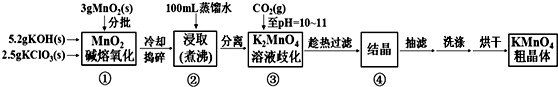
(1)步骤①应在D中熔化,并用铁棒用力搅拌,以防结块.
A.烧杯 B.蒸发皿 C.瓷坩埚 D.铁坩埚
(2)①综合相关物质的化学性质及溶解度,步骤③中可以替代CO2的试剂是B.
A.二氧化硫 B.稀醋酸 C.稀盐酸 D.稀硫酸
②当溶液pH值达10~11时,停止通CO2;若CO2过多,造成的后果是二氧化碳和碳酸钾反应生成碳酸氢钾,结晶时会同高锰酸钾一起析出,产品纯度降低.
(3)烘干时,温度控制在80℃为宜,理由是如果温度过低,烘干时间过长,如果温度过高,高锰酸钾受热分解.
(4)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极.请写出阳极的电极反应式MnO42--e-═MnO4-,与原方法相比,电解法的优势为K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率.
(5)通过用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数).
①量取KMnO4溶液应选用酸式(填“酸式”或“碱式”)滴定管;若量取KMnO4溶液的滴定管用蒸馏水洗净后未润洗,则最终测定结果将偏小(填“偏大”、“偏小”或“不变”).
②滴定过程中反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.(已知:常温下0.01mol/L的H2C2O4溶液的pH为2.1).
MnO2熔融氧化:3MnO2+KClO3+6KOH$\frac{\underline{\;熔化\;}}{\;}$3K2MnO4+KCl+3H2O
K2MnO4歧化:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
相关物质的溶解度数据见下表:
| 20℃ | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| s(g/100g水) | 111 | 33.7 | 11.1 | 6.34 |
请回答:

(1)步骤①应在D中熔化,并用铁棒用力搅拌,以防结块.
A.烧杯 B.蒸发皿 C.瓷坩埚 D.铁坩埚
(2)①综合相关物质的化学性质及溶解度,步骤③中可以替代CO2的试剂是B.
A.二氧化硫 B.稀醋酸 C.稀盐酸 D.稀硫酸
②当溶液pH值达10~11时,停止通CO2;若CO2过多,造成的后果是二氧化碳和碳酸钾反应生成碳酸氢钾,结晶时会同高锰酸钾一起析出,产品纯度降低.
(3)烘干时,温度控制在80℃为宜,理由是如果温度过低,烘干时间过长,如果温度过高,高锰酸钾受热分解.
(4)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极.请写出阳极的电极反应式MnO42--e-═MnO4-,与原方法相比,电解法的优势为K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率.
(5)通过用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数).
①量取KMnO4溶液应选用酸式(填“酸式”或“碱式”)滴定管;若量取KMnO4溶液的滴定管用蒸馏水洗净后未润洗,则最终测定结果将偏小(填“偏大”、“偏小”或“不变”).
②滴定过程中反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.(已知:常温下0.01mol/L的H2C2O4溶液的pH为2.1).
2.x、y、z三种物质的分子组成分别符合烷烃、烯烃、炔烃的通式,若在一定条件下V L的x、y、z的混合气体可与V L的H2发生加成反应,则混合气体中x、y、z的体积比不可能是( )
| A. | 1:1:1 | B. | 3:2:3 | C. | 1:4:1 | D. | 3:2:1 |
19.正丁烷的二氯取代产物有几种( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
9.1999年1月,俄美科学家联合小组宣布合成出114号元素中的一种同位素,该同位素原子的质量数为298.以下叙述不正确的是( )
| A. | 该元素属于第6周期 | |
| B. | 该元素位于IVA族 | |
| C. | 该元素为金属元素,性质与82Pb(铅)相似 | |
| D. | 该元素原子含有114个电子和184个中子 |
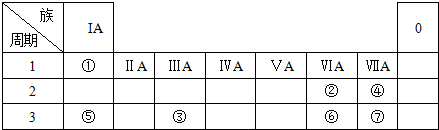
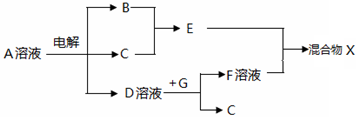
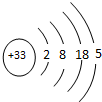 ,
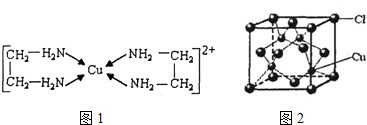
,
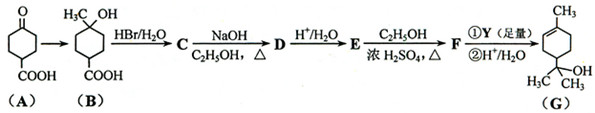
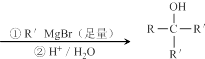
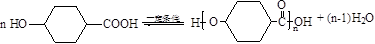 .
. .
. .
.
