题目内容
0.3mol气态高能燃料乙硼烷B2H6在O2中燃烧,生成固态B2O3和液态H2O,放出649.5kJ的热量.下列热化学方程式正确的是( )
| A、B2H6(g)+302(g)═B2O3(s)+3H2O(l)△H=2165 kJ?mol-1 |
| B、B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2165 kJ?mol-1 |
| C、B2H6+3O2═B2O3+3H2O△H=-2165 kJ?mol-1 |
| D、B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2165 kJ?mol-1 |
考点:有关反应热的计算,热化学方程式
专题:化学反应中的能量变化
分析:0.3mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5KJ的热量,则1mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出2165KJ的热量,根据盖斯定律写出其热化学反应方程式,后根据物质的物质的量与反应放出的热量成正比来解答.
解答:
解:0.3mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5KJ的热量,则1mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出2165KJ的热量,反应的热化学方程式为:B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2165kJ/mol,
A.热化学方程式中放热△H<0,△H>0表示吸热,而乙硼烷燃烧放热,故A错误;
B.0.3mol气态高能燃料乙硼烷在氧气中燃烧,放出649.5KJ的热量,则1mol气态高能燃料乙硼烷在氧气中燃烧,放出
=2165KJ,故B正确;
C.热化学方程式中没有标出物质的聚集状态,故C错误;
D.1mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和气态水,放出热量应小于2165 kJ,故D错误;
故选B.
A.热化学方程式中放热△H<0,△H>0表示吸热,而乙硼烷燃烧放热,故A错误;
B.0.3mol气态高能燃料乙硼烷在氧气中燃烧,放出649.5KJ的热量,则1mol气态高能燃料乙硼烷在氧气中燃烧,放出
| 649.5KJ |
| 0.3 |
C.热化学方程式中没有标出物质的聚集状态,故C错误;
D.1mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和气态水,放出热量应小于2165 kJ,故D错误;
故选B.
点评:本题考查了热化学方程式书写,需要注意的有:反应热的数值与化学方程式前面的系数成正比,题目较简单.注意热化学方程式的书写注意事项.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知下列两个热化学方程式
2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2220kJ/mol
实验测得氢气和丙烷的混合气体共2mol,完全燃烧时放出热量2505.8kJ,则混合气体中氢气和丙烷的体积比约为( )
2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2220kJ/mol
实验测得氢气和丙烷的混合气体共2mol,完全燃烧时放出热量2505.8kJ,则混合气体中氢气和丙烷的体积比约为( )
| A、1:3 | B、1:4 |
| C、1:1 | D、3:1 |
设阿伏加德罗常数为NA,下列说法正确的是( )
| A、5.6 g Fe与足量盐酸反应,反应中转移的电子数为0.3NA |
| B、0.1 mol FeCl3完全水解转化为氢氧化铁胶体,生成0.1NA个胶粒 |
| C、常温下,28 g的N2和CO混合气体含有的原子数为2NA |
| D、常温下,1 L 0.1 mol/L Na2CO3溶液中,含有CO32-数为0.1NA |
下列实验操作或装置符合实验要求的是( )
A、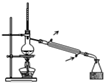 用如图装置可用于分离互不相溶的液体 |
B、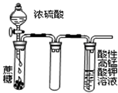 用如图装置酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
C、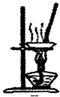 用如图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
D、 用如图确认CO2和NaOH已发生反应 |
下列各组物质互为同素异形体的是( )
| A、红磷与白磷 | ||||
| B、磷酸与偏磷酸 | ||||
| C、NO2与N2O4D | ||||
D、
|
同温同压下,下列各组化学方程式中Q2>Q1的是( )
| A、2H2(g)+O2(g)═2H2O(l)△H=-Q1kJ/mol 2H2(g)+O2(g)═2H2O(g)△H=-Q2kJ/mol | ||||
| B、S(g)+O2(g)═SO2(g)△H=-Q1kJ/mol S(s)+O2(g)═SO2(g)△H=-Q2kJ/mol | ||||
| C、C(s)+1/2O2(g)═CO(g)△H=-Q1kJ/mol C(s)+O2(g)═CO2(g)△H=-Q2kJ/mol | ||||
D、H2(g)+Cl2(g)═2HCl(g)△H=-Q1kJ/mol
|
有八种物质①甲烷 ②苯 ③聚乙烯 ④丙烯 ⑤乙炔 ⑥丁烷 ⑦邻二甲苯 ⑧二氧化硫,既能使酸性高锰酸钾溶液褪色又能与溴水反应的是( )
| A、④⑤⑧ | B、③④⑤⑧ |
| C、④⑤⑦⑧ | D、③④⑤⑦⑧ |
设NA表示阿伏加德罗常数数值,下列叙述中正确的是( )
| A、标准状况下,11.2 L氦气所含的原子数为NA |
| B、标准状况下,11.2g氢气所含的原子数约为5.6 NA |
| C、常温常压下,48 g O3含有的氧原子数约为3NA |
| D、36.5g HCl中含有的氯原子数为0.2NA |