题目内容
设NA表示阿伏加德罗常数数值,下列叙述中正确的是( )
| A、标准状况下,11.2 L氦气所含的原子数为NA |
| B、标准状况下,11.2g氢气所含的原子数约为5.6 NA |
| C、常温常压下,48 g O3含有的氧原子数约为3NA |
| D、36.5g HCl中含有的氯原子数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.稀有气体为单原子分子,0.5mol氦气中含有0.5mol氦原子;
B.11.2g氢气的物质的量为5.6mol,含有11.2mol氢原子;
C.臭氧中只含有氧原子,48g臭氧中含有48g氧原子,含有3mol氧原子;
D.36.5g氯化氢的物质的量为1mol,1mol氯化氢分子中含有1mol氯原子.
B.11.2g氢气的物质的量为5.6mol,含有11.2mol氢原子;
C.臭氧中只含有氧原子,48g臭氧中含有48g氧原子,含有3mol氧原子;
D.36.5g氯化氢的物质的量为1mol,1mol氯化氢分子中含有1mol氯原子.
解答:
解:A.标况下,11.2L氦气的物质的量为::
=0.5mol,0.5mol氦气分子中含有0.5mol氦原子,所含的原子数为0.5NA,故A错误;
B.11.2g氢气的物质的量为:
=5.6mol,5.6mol氢气中含有11.2mol氢原子,所含的原子数约为11.2NA,故B错误;
C.48g臭氧中含有48g氧原子,48g氧原子中含有3mol氧原子,含有的氧原子数约为3NA,故C正确;
D.36.5g HCl中含有1mol氯化氢,含有1mol氯原子,含有的氯原子数为NA,故D错误;
故选C.
| 11.2L |
| 22.4L/mol |
B.11.2g氢气的物质的量为:
| 11.2g |
| 2g/mol |
C.48g臭氧中含有48g氧原子,48g氧原子中含有3mol氧原子,含有的氧原子数约为3NA,故C正确;
D.36.5g HCl中含有1mol氯化氢,含有1mol氯原子,含有的氯原子数为NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
0.3mol气态高能燃料乙硼烷B2H6在O2中燃烧,生成固态B2O3和液态H2O,放出649.5kJ的热量.下列热化学方程式正确的是( )
| A、B2H6(g)+302(g)═B2O3(s)+3H2O(l)△H=2165 kJ?mol-1 |
| B、B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2165 kJ?mol-1 |
| C、B2H6+3O2═B2O3+3H2O△H=-2165 kJ?mol-1 |
| D、B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2165 kJ?mol-1 |
下列化学方程式正确的是( )
A、S+O2
| ||||
B、4Al+3O2
| ||||
C、P+O2
| ||||
D、Mg+O2
|
下列事实能说明苯环中不存在单双键交替的是( )
| A、苯不能使酸性KMnO4溶液褪色 |
| B、苯在一定条件下可与液溴发生取代反应 |
| C、苯在一定条件下可与H2发生加成反应 |
| D、苯不能使溴水褪色 |
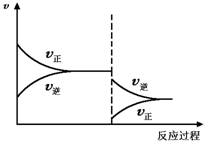 如图表示在某容器中,充入N2和H2,在一定条件下N2+3H2?2NH3△H<0的反应达到平衡,当条件改变时原平衡被破坏,反应一段时间后又建立起新的平衡.符合该图变化的条件是( )
如图表示在某容器中,充入N2和H2,在一定条件下N2+3H2?2NH3△H<0的反应达到平衡,当条件改变时原平衡被破坏,反应一段时间后又建立起新的平衡.符合该图变化的条件是( )| A、可逆反应达到平衡后,将NH3液化并建立新的平衡 |
| B、可逆反应达到平衡后,再减小压强并建立新的平衡 |
| C、可逆反应达到平衡后,再降低温度并建立新的平衡 |
| D、可逆反应达到平衡后,再升高温度并建立新的平衡 |
下列有关化学实验的描述中正确的是( )
| A、分离乙醇和乙酸要用分液的方法 |
| B、配制一定物质的量浓度的NaCl溶液,如果NaCl固体中含有Na2CO3,所配制溶液中c(Na+)将偏高 |
| C、某无色溶液中加稀硫酸产生无色无味气体,该气体能使澄清石灰水变浑浊,说明该溶液中含CO32- |
| D、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
下列关于常见有机化合物的说法中,正确的是( )
| A、乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应 |
| B、甲烷和苯都不能使酸化的KMnO4溶液褪色,也均不能发生氧化反应 |
| C、乙醇、乙酸、乙酸乙酯都能发生取代反应 |
| D、糖类、油脂和蛋白质都是人体必需的营养物质,它们的组成元素相同 |
氮气常用作保护气,其原因是( )
| A、氮气在任何条件下不与其他物质发生化学反应 |
| B、氮气比氧气稳定 |
| C、氮气是双原子分子 |
| D、氮气分子中的N≡N键很牢固 |
下列说法正确的是( )
A、钾(K)原子基态的原子结构示意图为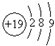 |
B、H2O电子式为 |
| C、Mg的原子基态电子排布式为1s22s22p63s23p1 |
| D、Ca原子基态电子排布式为1s22s22p63s23p6 |