题目内容
已知下列两个热化学方程式
2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2220kJ/mol
实验测得氢气和丙烷的混合气体共2mol,完全燃烧时放出热量2505.8kJ,则混合气体中氢气和丙烷的体积比约为( )
2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2220kJ/mol
实验测得氢气和丙烷的混合气体共2mol,完全燃烧时放出热量2505.8kJ,则混合气体中氢气和丙烷的体积比约为( )
| A、1:3 | B、1:4 |
| C、1:1 | D、3:1 |
考点:有关反应热的计算
专题:计算题,化学反应中的能量变化
分析:先根据方程式求出H2和C3H8的燃烧热,设H2的物质的量为nmol,则C3H8的物质的量为2mol-n,根据放出的热量列方程式解答.
解答:
解:设混合气中H2的物质的量为n,则C3H8的物质的量为2mol-n.根据题意,列方程为:
kJ/mol×n+2220.0kJ/mol×(2mol-n)=2505.8kJ
解得 n=1mol;C3H8的物质的量为2mol-1mol=1mol.
所以混合气体中H2与C3H8的体积比即物质的量之比为1mol:1mol=1:1.
故选C.
| 571.6 |
| 2 |
解得 n=1mol;C3H8的物质的量为2mol-1mol=1mol.
所以混合气体中H2与C3H8的体积比即物质的量之比为1mol:1mol=1:1.
故选C.
点评:本题考查反应热的有关计算,题目难度不大,关键是注意反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比.

练习册系列答案
相关题目
阿司匹林是一种常见药物,它的相对分子质量为180,含碳、氢、氧三种元素,其中碳、氢的质量数分别是60%、4.4%,则阿司匹林的分子式是( )
| A、C10H9O4 |
| B、C 10H22O3 |
| C、C9H10O4 |
| D、C9H8O4 |
与键线式为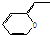 的物质互为同分异构体的是( )
的物质互为同分异构体的是( )
 的物质互为同分异构体的是( )
的物质互为同分异构体的是( )A、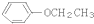 |
B、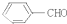 |
C、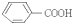 |
D、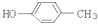 |
常温下,下列不能共存的分子组( )
| A、N2、O2、CO2、H2 |
| B、N2、H2、H2O(g)、CO |
| C、NH3、Cl2、HCl、H2 |
| D、CO、CO2、O2、HCl |
0.3mol气态高能燃料乙硼烷B2H6在O2中燃烧,生成固态B2O3和液态H2O,放出649.5kJ的热量.下列热化学方程式正确的是( )
| A、B2H6(g)+302(g)═B2O3(s)+3H2O(l)△H=2165 kJ?mol-1 |
| B、B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2165 kJ?mol-1 |
| C、B2H6+3O2═B2O3+3H2O△H=-2165 kJ?mol-1 |
| D、B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2165 kJ?mol-1 |
下列化学方程式正确的是( )
A、S+O2
| ||||
B、4Al+3O2
| ||||
C、P+O2
| ||||
D、Mg+O2
|