题目内容
12.在一定条件下,向5L密闭容器中充入2molA气体和1mol B气体,发生可逆反应:2A(g)+B(g)?2C(g),达到平衡时容器内B的浓度为0.1mol/L,则B的转化率为( )| A. | 67% | B. | 50% | C. | 25% | D. | 10% |
分析 达到平衡时容器内B的浓度为0.1mol/L,则由n=cV可计算B平衡时的物质的量,再根据转化率=$\frac{物质的转化量}{物质的起始量}$×100%,以此解答该题.
解答 解:平衡时B的物质的量为0.1mol/L×5L=0.5mol,参加反应的B有1mol,则B的转化率为:$\frac{B的转化量}{B的起始量}$×100%=$\frac{1mol-0.5mol}{1mol}$×100%=50%;
故选B.
点评 本题考查了化学平衡的计算应用,反应物转化率的计算应用,为高频考点,侧重于学生的分析能力的考查,注意单位的统一,题目较简单.

练习册系列答案
相关题目
17.下列过程中,不涉及化学变化的是( )
| A. | 用食醋除水垢 | |
| B. | 甘油加水作护肤剂 | |
| C. | 双氧水漂白美容 | |
| D. | 烹鱼时,加入少量的料酒和食醋可减少腥味,增加香味 |
15.25℃、101kPa下,4g CH4完全燃烧生成CO2和液态H2O时,放出222.5kJ的热量,则下列热化学方程式中正确的是( )
| A. | CH4(g)+2O2(g)=CO2(g)+4H2O(g)△H=-890 kJ/mol | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890 kJ/mol | |
| C. | CH4(g)+2O2(g)=CO2(g)+H2O(l)△H=-445 kJ/mol | |
| D. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890 kJ/mol |
7.CO2是目前大气中含量最高的一种温室气体.因此,控制和治理CO2是解决温室效应的有效途径.
已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)?FeO(s)+H2(g)的平衡常数为K2.
在不同温度时K1、K2的值如下表:
(1)推导反应CO2(气)+H2(气)?CO(气)+H2O(气)的平衡常数K与K1、K2的关系式:K=$\frac{{K}_{1}}{{K}_{2}}$.
(2)通过K值的计算,(1)中的反应是吸热反应(填“吸热”或“放热”).
(3)在一体积为10L的密闭容器中,加入一定量的CO2和H2O(气),在1173开时发生反应并记录前5min的浓度,第6min时改变了反应的条件.各物质的浓度变化如下表:
①前2min,用CO表示的该化学反应的速率是:v(CO)=0.0130mol•L-1•nin-1.
②在3~4min之间,反应处于平衡状态(填“平衡”或“非平衡”).
③第6min时,平衡向正反应方向移动,可能的原是升高温度或降低了H2浓度.
已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)?FeO(s)+H2(g)的平衡常数为K2.
在不同温度时K1、K2的值如下表:
| 温度(绝对温度) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
(2)通过K值的计算,(1)中的反应是吸热反应(填“吸热”或“放热”).
(3)在一体积为10L的密闭容器中,加入一定量的CO2和H2O(气),在1173开时发生反应并记录前5min的浓度,第6min时改变了反应的条件.各物质的浓度变化如下表:
| 时间/min | CO2 | H2O | CO | H2 |
| 0 | 0.2000 | 0.3000 | 0 | 0 |
| 2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | |
| 5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
| 6 | 0.0350 | 0.1350 | 0.1650 |
②在3~4min之间,反应处于平衡状态(填“平衡”或“非平衡”).
③第6min时,平衡向正反应方向移动,可能的原是升高温度或降低了H2浓度.
2.下列化学变化中,物质发生还原反应的是( )
| A. | C→CO2 | B. | CO2→CO | C. | FeCl2→FeCl3 | D. | H2SO4→BaSO4 |
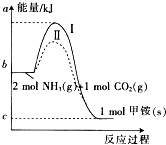 氨基甲酸铵(NH2COONH4,简称甲铵)是CO2和NH3制尿素的中间产物,其中CO2反应生成甲铵的能量变化如图所示.
氨基甲酸铵(NH2COONH4,简称甲铵)是CO2和NH3制尿素的中间产物,其中CO2反应生成甲铵的能量变化如图所示.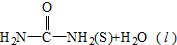 △H=+dkJ•mol-1,则由CO2(g)和NH3(g)直接合成固态尿素并生成液态水的热化学方程式为CO2(g)+2NH3(g)=
△H=+dkJ•mol-1,则由CO2(g)和NH3(g)直接合成固态尿素并生成液态水的热化学方程式为CO2(g)+2NH3(g)=