题目内容
4.天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷.(1)工业上可用煤制天然气,生产过程中有多种途径生成CH4.
已知:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41kJ•mol-1
C(s)+2H2(g)?CH4(g)△H=-73kJ•mol-1
2CO(g)?C(s)+CO2(g)△H=-171kJ•mol-1
则CO与H2反应生成CH4(g)和H2O(g)的热化学方程式为CO (g)+3H2(g)═CH4(g)+H2O(g)△H=-203kJ•mol-1.
(2)天然气中的H2S杂质常用氨水吸收,产物为NH4HS.一定条件下向NH4HS溶液中通入空气,得到单质硫并再生出吸收液,则该反应的化学方程式为2NH4HS+O2$\frac{\underline{\;一定条件\;}}{\;}$2NH3•H2O+2S↓.
(3)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g)?2CO(g)+2H2(g).在密闭容器中通入物质的量浓度均为0.1mol•L-1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图1所示,则压强P1<P2(填“>”或“<”);压强为P2时,在Y点:v(正)>v(逆)(填“>”、“<”或“=”);写出X点对应温度下的该反应的平衡常数计算式K=$\frac{0.1{6}^{2}×0.1{6}^{2}}{0.02×0.02}$(不必计算出结果).

(4)以二氧化钛表面覆盖CuAl2O4为催化剂,可以将CH4和CO2直接转化成乙酸.
①在不同温度下催化剂的催化效率与乙酸的生成速率如图2所示.在275~400℃之间,乙酸的生成速率先降低后升高的原因是温度在275°C升至300°C时,达平衡后催化剂催化效率降低的因素超过了温度升高使速率增大的因素,所以乙酸生成速率降低;当温度由300o升至400oC时,温度升高使反应速率增大的因素超过了催化剂催化效率降低的因素,所以乙酸的生成速率又增大.
②为了提高该反应中CH4的转化率,可以采取的措施是增大反应压强或增大CO2的浓度(写一条).
③乙酸(用HAc表示)电离方程式为HAc?H++Ac-,电离常数用Ka表示;乙酸根的水解方程式为Ac-+H2O?OH-+HAc,水解常数用Kh表示,则Kh=$\frac{Kw}{Ka}$(用Ka和水的离子积KW表示).
分析 (1)①CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41kJ•mol-1
②C(s)+2H2(g)?CH4(g)△H=-73kJ•mol-1
③2CO(g)?C(s)+CO2(g)△H=-171kJ•mol-1
依据盖斯定律计算,②+③-①得到CO与H2反应生成CH4(g)和H2O(g)的热化学方程式;
(2)根据元素守恒和电子得失守恒写出化学方程式;
(3)温度一定时,增大压强平衡逆向移动,甲烷的转化率减小;
Y点甲烷转化率小于同温同压下平衡时转化率,故Y点向正反应进行建立平衡;
温度为1100℃,压强为P2时甲烷的转化率为80%,则平衡时甲烷浓度变化量为0.1mol•L-1×70%=0.1mol,计算平衡时各组分浓度,代入K=$\frac{{c}^{2}(CO){c}^{2}({H}_{2})}{c(C{O}_{2})c(C{H}_{4})}$计算平衡常数;
(4)①由图可知,温度超过275~300℃时,催化剂的催化效率降低,所以温度升高而乙酸的生成速率降低;300~400℃时温度升高,化学反应速率加快;
②提高该反应中CH4的转化率,改变条件应使平衡向正反应方向移动,注意不能只增大甲烷的浓度,否则甲烷的转化率降低;
③写出醋酸电离平衡常数、醋酸根离子水解平衡常数,水的离子积常数进行比较,从而得出结论.
解答 解:(1)(1)①CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41kJ•mol-1
②C(s)+2H2(g)?CH4(g)△H=-73kJ•mol-1
③2CO(g)?C(s)+CO2(g)△H=-171kJ•mol-1
依据盖斯定律计算,②+③-①得到CO与H2反应生成CH4(g)和H2O(g)的热化学方程式为:CO(g)+3H2(g)?CH4(g)+H2O(g)△H=-203kJ•mol-1;
故答案为:CO (g)+3H2(g)═CH4(g)+H2O(g)△H=-203kJ•mol-1;
(2)根据元素守恒及题中的反应物和生成物可知化学方程式为:2NH4HS+O2$\frac{\underline{\;一定条件\;}}{\;}$2NH3•H2O+2S↓,
故答案为:2NH4HS+O2$\frac{\underline{\;一定条件\;}}{\;}$2NH3•H2O+2S↓;
(3)温度一定时,增大压强平衡逆向移动,甲烷的转化率减小,故压强P1<P2;Y点甲烷转化率小于同温同压下平衡时转化率,故Y点向正反应进行建立平衡,则v(正)>v(逆);温度为1100℃,压强为P2时甲烷的转化率为80%,则平衡时甲烷浓度变化量为0.1mol•L-1×80%=0.08mol,则:
CO2(g)+CH4(g)?2CO(g)+2H2(g),
开始 0.1 0.1 0 0
转化 0.08 0.08 0.16 0.16
平衡 0.02 0.02 0.16 0.16
故平衡常数K=$\frac{{c}^{2}(CO){c}^{2}({H}_{2})}{c(C{O}_{2})c(C{H}_{4})}$=$\frac{0.1{6}^{2}×0.1{6}^{2}}{0.02×0.02}$
故答案为:<;>;$\frac{0.1{6}^{2}×0.1{6}^{2}}{0.02×0.02}$;
(4)①在不同温度下催化剂的催化效率与乙酸的生成速率如图2所示.在275~400℃之间,乙酸的生成速率先降低后升高的原因是:温度在275°C升至300°C时,达平衡后催化剂催化效率降低的因素超过了温度升高使速率增大的因素,所以乙酸生成速率降低;当温度由300o升至400oC时,温度升高使反应速率增大的因素超过了催化剂催化效率降低的因素,所以乙酸的生成速率又增大,
故答案为:温度在275°C升至300°C时,达平衡后催化剂催化效率降低的因素超过了温度升高使速率增大的因素,所以乙酸生成速率降低;当温度由300o升至400oC时,温度升高使反应速率增大的因素超过了催化剂催化效率降低的因素,所以乙酸的生成速率又增大;
②提高该反应中CH4的转化率,改变条件应使平衡向正反应方向移动,正反应是气体体积减小的反应,缩小容器体积增大压强、增大CO2的浓度,平衡正向移动,反应物转化率增大,
故答案为:增大反应压强或增大CO2的浓度;
③电离方程式为HAc?H++Ac-,电离常数用Ka=$\frac{c(A{c}^{-})c({H}^{+})}{c(HAc)}$,乙酸根的水解方程式为Ac-+H2O?OH-+HAc,水解常数用Kh=$\frac{c(HAc)c(O{H}^{-})}{c(A{c}^{-})}$,Kw=c(H+).c(OH-),${K_h}=\frac{{c(O{H^-})•c(HAc)}}{{c(A{c^-})•c({H_2}O)}}=\frac{{c(O{H^-})•c(HAc)}}{{c(A{c^-})•c({H_2}O)}}•\frac{{c({H^+})}}{{c({H^+})}}=\frac{{c(O{H^-})•c({H^+})}}{{c({H_2}O)}}•\frac{c(HAc)}{{c(A{c^-})•c({H^+})}}=\frac{K_W}{K_a}$,
故答案为:$\frac{Kw}{Ka}$.
点评 本题考查了盖斯定律的应用、方程式的书写、化学平衡常数、平衡移动等,题目涉及的知识点较多,侧重于考查学生对基础知识的综合应用能力,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | K | B. | Ca | C. | Na | D. | Fe |
| A. | 35Cl原子所含质子数为18 | |
| B. | 1mol的1H35Cl分子所含中子数为18个 | |
| C. | 7g的35Cl2气体的体积为2.24L | |
| D. | 35Cl2气体的摩尔质量为70g/mol |
| A. | 67% | B. | 50% | C. | 25% | D. | 10% |
N2(g)+2O2(g)═2NO2(g);△H=+67.7kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g);△H=-534kJ/mol
下列关于肼和NO2反应的热化学方程式中,正确的是( )
| A. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l);△H=-1135.7 kJ/mol | |
| B. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g);△H=-1000.3 kJ/mol | |
| C. | N2H4(g)+NO2(g)═N2(g)+2H2O(l);△H=-1135.7 kJ/mol | |
| D. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g);△H=-1135.7 kJ/mol |
①40mL 0.03mol/L的盐酸;
②50mL 0.03mol/L的硝酸银溶液;?
③30mL 0.02mol/L的氯化钙溶液;
④10mL蒸馏水.
AgCl在四种溶液中的溶解度顺序为( )
| A. | ?④>①=②>③ | B. | ?④>①>②=③ | C. | ?④=①>②>③ | D. | ?①=②>④>③ |
| A. | 蒸馏 | B. | 分液 | C. | 过滤 | D. | 蒸发 |
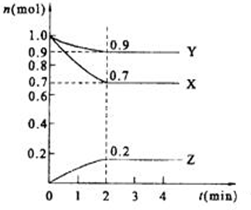 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.