题目内容
2.已知自然界氧的核素有16O、8O,氢的核素有 H、D,从水分子的原子组成来看,自然界的水一共有( )| A. | 3种 | B. | 6种 | C. | 9种 | D. | 12种 |
分析 氢的核素有H、D,氧的核素有16O、18O,根据水分子是由2个氢原子和1个氧原子构成,书写出水可能的分子式,依此进行判断.
解答 解:氢的核素有H、D,氧的核素有16O、18O,故水的分子式可能为:H216O、D216O、H218O、D218O、HD16O、HD18O,共6种,
故选B.
点评 本题考查同位素的有关知识,难度不大.要注意基础知识的积累.

练习册系列答案
相关题目
12.从化学键角度分析,下列属于化学变化的是( )
| A. | 蔗糖溶解 | B. | H2SO4溶于水 | C. | NH3溶于水 | D. | 氯化镁受热熔化 |
10.溴有两种同位素,在自然界中这两种同位素大约各占一半,已知溴的原子序数是35,原子量是80,则溴的两种同位素的中子数分别等于( )
| A. | 79、81 | B. | 45、46 | C. | 44、45 | D. | 44、46 |
17.某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.已知:p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lgc(SO42-).下列说法正确的是( )


| A. | 该温度下,Ksp (BaSO4 )=1.0×10-24 | |
| B. | a点的Ksp (BaSO4 )小于b点的Ksp (BaSO4 ) | |
| C. | d点表示的是该温度下BaSO4的不饱和溶液 | |
| D. | 加入BaCl2可以使溶液由 c点变到a点 |
7.下列分子中所有原子都满足最外层8电子结构的是( )
| A. | BeCl2 | B. | PCl3 | C. | PCl5 | D. | H2O |
14.第三周期元素X的原子要实现最外层8电子稳定结构,所需的电子数小于次外层和最内层的电子数之差,且等于最内层电子数的整数倍.下列说法正确的是( )
| A. | X元素最高价氧化物对应的水化物一定是强酸 | |
| B. | X元素氢化物的化学式一定为H2X | |
| C. | X的单质一定是良好的半导体材料 | |
| D. | X元素的氧化物一定能与烧碱反应 |
11.将一定量的锌与100mL 18.5mol/L浓硫酸充分反应后,锌完全溶解,同时生成气体A为33.6L(标准状况).将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol•L-1,则下列叙述中错误的是( )
| A. | 气体A为SO2和H2的混合物 | B. | 气体A中SO2和H2的体积比为4:1 | ||
| C. | 反应中共消耗Zn 97.5g | D. | 反应中共转移3mol电子 |
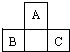 A、B、C为短周期元素,它们的位置关系如图所示,已知B、C两元素原子序数之和是A元素的原子序数的4倍,则
A、B、C为短周期元素,它们的位置关系如图所示,已知B、C两元素原子序数之和是A元素的原子序数的4倍,则 ,A的氢化物分子式为H2O;
,A的氢化物分子式为H2O;