题目内容
7.下列关于物质检验的说法正确的是( )| A. | 加入氯化钡溶液有白色沉淀生成,再加稀盐酸,沉淀不消失,则原溶液中一定有SO42- | |
| B. | 加入烧碱溶液后加热,产生能使湿润红色石蕊试纸变蓝的气体,则原溶液中一定有NH4+ | |
| C. | 加入盐酸,放出能使澄淸石灰水变浑浊的无色气体,则原溶液中一定有CO32- | |
| D. | 加入AgNO3溶液,有白色沉淀生成,则原溶液中一定含有NaCl |
分析 A.白色沉淀可能为AgCl;
B.氨气能使湿润红色石蕊试纸变蓝;
C.气体可能为二氧化碳或二氧化硫;
D.白色沉淀为AgCl、硫酸银或碳酸银等.
解答 解:A.白色沉淀可能为AgCl,则原溶液中不一定有SO42-,故A错误;
B.氨气能使湿润红色石蕊试纸变蓝,则原溶液中一定有NH4+,故B正确;
C.气体可能为二氧化碳或二氧化硫,则原溶液中可能有CO32-或SO32-,或HCO3-等,故C错误;
D.白色沉淀为AgCl、硫酸银或碳酸银等,则溶液中可能含NaCl,故D错误;
故选B.
点评 本题考查常见离子的检验,为高频考点,把握离子检验的试剂、现象、结论为解答的关键,侧重分析与应用能力的考查,注意检验时排除干扰离子,题目难度不大.

练习册系列答案
相关题目
18.某温度下,在密闭容器中发生如下反应:2A(g)+B(g)?2C(g),开始时充入2mol C气体,达到平衡时,混合气体的压强比起始时增大了20%,则达平衡时C的转化率为( )
| A. | 80% | B. | 60% | C. | 40% | D. | 20% |
15.短周期主族元素X、Y、Z、W的原子序数依次增大.X、Y、Z、W最外层电子数之和为16,Y 原子的最外层电子数是其内层电子数的3 倍,Z2+ 与Y2- 具有相同的电子层结构,W 与X 同主族.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Y 分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X 的最高价氧化物对应的水化物的酸性比W 的弱 | |
| D. | Y 的气态简单氢化物的热稳定性比W 的强 |
2.下列图示实验能达到实验目的是( )
| A. | 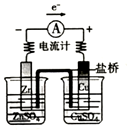 探究原电池原理 | B. | 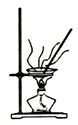 制备无水氯化铁 | ||
| C. | 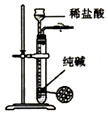 制取少量纯净的CO2气体 | D. | 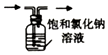 收集氨气 |
12.硅是制造芯片和半导体的材料.下列关于${\;}_{14}^{29}$Si的叙述正确的是( )
| A. | 质子数是29 | B. | 中子数是14 | C. | 电子数是14 | D. | 质量数是15 |
19. 甲、乙、丙中均含有某种相同的元素,与试剂m、n完成如图的转化关系,反应条件及部分产物省略.下列假设与推断不成立的是( )
甲、乙、丙中均含有某种相同的元素,与试剂m、n完成如图的转化关系,反应条件及部分产物省略.下列假设与推断不成立的是( )
 甲、乙、丙中均含有某种相同的元素,与试剂m、n完成如图的转化关系,反应条件及部分产物省略.下列假设与推断不成立的是( )
甲、乙、丙中均含有某种相同的元素,与试剂m、n完成如图的转化关系,反应条件及部分产物省略.下列假设与推断不成立的是( )| 选项 | 假设 | 结论 |
| A | 甲为N2 | n可能是O2 |
| B | 甲为FeCl2溶液 | m可能是Cl2 |
| C | 甲为AlCl3溶液 | m可能是NaOH溶液 |
| D | 甲为Na2CO3溶液 | n可能是CO2 |
| A. | A | B. | B | C. | C | D. | D |
16.在周期表中短周期主族元素X、Y、Z、W,它们的原子序数依次增大.X与Z同主族,X与Z的原子序数之和为24.W原子的最外层电子数比Y原子的最外层电子数多2个.下列叙述正确的是( )
| A. | 气态氢化物的稳定性 Z>X | B. | 最高价氧化物的水化物酸性Z>W | ||
| C. | Z的氧化物不止一种 | D. | 原子半径 Z>Y |
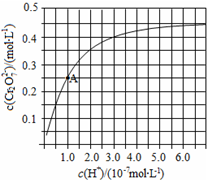 铬是用途广泛的金属元素.
铬是用途广泛的金属元素.