题目内容
2.下列图示实验能达到实验目的是( )| A. | 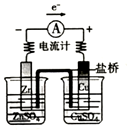 探究原电池原理 | B. | 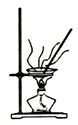 制备无水氯化铁 | ||
| C. | 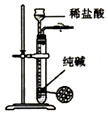 制取少量纯净的CO2气体 | D. | 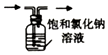 收集氨气 |
分析 A.图中装置可构成原电池,Zn为负极,电子由负极流向正极;
B.蒸发时氯化铁水解,生成的盐酸易挥发;
C.纯碱为粉末固体,与盐酸混合后不能分离;
D.氨气极易溶于水.
解答 解:A.图中装置可构成原电池,Zn为负极,电子由负极流向正极,图中装置可探究原电池原理,故A正确;
B.蒸发时氯化铁水解,生成的盐酸易挥发,则蒸干不能得到氯化铁,故B错误;
C.纯碱为粉末固体,与盐酸混合后不能分离,则不能用于制备少量气体,应选碳酸钙与盐酸制备,故C错误;
D.氨气极易溶于水,图中装置不能收集氨气,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、原电池、盐类水解、气体的制备和收集、实验技能为解答的关键,侧重分析与实验能力的考查,题目难度不大,注意实验的评价性分析.

练习册系列答案
相关题目
12.下列叙述不正确的是( )
| A. | 工业上用电解法冶炼钠、镁、铝等活泼金属 | |
| B. | 粗铜精炼时,与电源负极相连的是纯铜,该电极反应式为Cu2++2e-=Cu | |
| C. | 由C(s,石墨)=C(s,金刚石)△H=+1.9kJ/mol可知,金刚石比石墨稳定 | |
| D. | 反应SO2(g)+2H2S(g)=3S (s)+2H2O(l)在常温下能自发进行,则该反应的△H<0 |
13.CO(g)与H2O(g)反应过程的能量变化如图所示,有关两者反应的说法中正确的是( )


| A. | 该反应为吸热反应 | |
| B. | CO(g)和H2O(g)所具有的总能量大于CO2(g)和H2(g)所具有的总能量 | |
| C. | 反应的热化学方程式:CO(g)+H2O(g)═CO2(g)+H2(g)△H=41 kJ•mol-1 | |
| D. | 1 mol CO2(g)和1 mol H2(g)反应生成1 mol CO(g)和H2O(g)要放出41 kJ的热量 |
7.下列关于物质检验的说法正确的是( )
| A. | 加入氯化钡溶液有白色沉淀生成,再加稀盐酸,沉淀不消失,则原溶液中一定有SO42- | |
| B. | 加入烧碱溶液后加热,产生能使湿润红色石蕊试纸变蓝的气体,则原溶液中一定有NH4+ | |
| C. | 加入盐酸,放出能使澄淸石灰水变浑浊的无色气体,则原溶液中一定有CO32- | |
| D. | 加入AgNO3溶液,有白色沉淀生成,则原溶液中一定含有NaCl |
14.下列关于NO的说法中,不正确的是( )
| A. | 是红棕色有刺激性气味的气体 | |
| B. | 在空气中极易被氧化生成NO2 | |
| C. | 在O2存在时能与水发生反应生成硝酸 | |
| D. | 可由NH3在催化剂作用下与O2反应生成 |
11.下列过程发生化学变化的是( )
| A. | 蜡烛照明 | B. | 太阳能供热 | ||
| C. | 用金刚石切割玻璃 | D. | 酒香扑鼻 |

 .
.