题目内容
 常温时,用1.0mol/L NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积关系如图所示.原硫酸溶液的物质的量浓度和完全反应后溶液的总体积是( )
常温时,用1.0mol/L NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积关系如图所示.原硫酸溶液的物质的量浓度和完全反应后溶液的总体积是( )| A、1 mol/L 60mL |
| B、0.5 mol/L 80mL |
| C、0.5 mol/L40mL |
| D、1 mol/L 80mL |
考点:化学方程式的有关计算
专题:计算题
分析:根据硫酸溶液的pH确定氢离子浓度,再根据硫酸和氢离子之间的关系式确定硫酸浓度;根据硫酸和氢氧化钠反应的关系式计算氢氧化钠溶液的体积,硫酸和氢氧化钠溶液体积就是完全反应后溶液的总体积.
解答:
解:根据图象知,硫酸的pH=0,则c(H+)=1mol/L,c(H2SO4)=
C(H+)=0.5mol/L;完全反应时氢氧化钠溶液的体积为40mL,根据反应中氢氧化钠和硫酸的关系式得:n(NaOH)=2n(H2SO4)=2×0.5mol/L×0.04L=1mol/L×V,所以V(NaOH)=
=40mL,则混合溶液体积=40mL×2=80mL,故选B.
| 1 |
| 2 |
| 2×0.5mol/L×0.04L |
| 1mol/L |
点评:本题考查了物质的量的有关计算,根据曲线中pH确定硫酸浓度,再结合硫酸和氢氧化钠的关系式进行解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
相同温度下,有体积相同、pH相等的烧碱溶液和氨水,下列叙述中正确的是( )
| A、两溶液物质的量浓度相同 |
| B、两溶液中OH-浓度相同 |
| C、用同浓度的盐酸中和时,消耗盐酸的体积相同 |
| D、加入等体积的水稀释后,pH仍相等 |
下列表示对应化学反应的离子方程式正确的是( )
| A、铜溶于FeCl3溶液:Cu+Fe3+=Cu2++Fe2+ |
| B、NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| C、次氯酸钠溶液中滴入浓盐酸产生氯气:ClO-+Cl-+2H+=Cl2↑+H2O |
| D、碳酸氢钙溶液中加入澄清石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
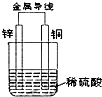 如图所示,将锌片和铜片通过导线相连,置于稀硫酸中.下列说法正确的是( )
如图所示,将锌片和铜片通过导线相连,置于稀硫酸中.下列说法正确的是( )| A、能将电能转换为化学能 |
| B、溶液会逐渐变为蓝色 |
| C、锌片是负极,发生氧化反应 |
| D、外电路中电子由铜片经导线流向锌片 |
标准状况下,2.8L氦气含有x个原子,则阿伏加德罗常数的值可表示为( )
A、
| ||
B、
| ||
| C、4x | ||
| D、8x |
 瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图,有关说法正确的是( )
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图,有关说法正确的是( )| A、电池总反应为:4NH3+3O2=2N2+6H2O |
| B、电池工作时,OH-向正极移动 |
| C、电极2发生的电极反应为:O2+4H++4e-=2H2O |
| D、电流由电极1经外电路流向电极2 |
2.7g铝粉分别与体积均为100mL、浓度均为2mol/L的(1)硫酸溶液、(2)烧碱溶液、(3)盐酸完全反应,放出氢气的体积关系(相同条件)是( )
| A、(1)=(2)=(3) |
| B、(1)=(2)>(3) |
| C、(1)>(2)>(3) |
| D、(2)>(1)=(3) |
 有两个起始体积相同的密闭容器A和B,A容器为固定体积;B容器有一个可移动的活塞,能使容器内保持恒压.起始时这两个容器分别充入等量的SO3气体,并使A、B容器中气体体积相等,并保持在400℃条件下发生反应2SO3?2SO2+O2,并达到平衡.
有两个起始体积相同的密闭容器A和B,A容器为固定体积;B容器有一个可移动的活塞,能使容器内保持恒压.起始时这两个容器分别充入等量的SO3气体,并使A、B容器中气体体积相等,并保持在400℃条件下发生反应2SO3?2SO2+O2,并达到平衡.