题目内容
4.镀锌铁在发生吸氧腐蚀时,若有0.2mol电子发生转移,下列说法正确的是( )①有5.6g金属被腐蚀
②有6.5g金属被腐蚀
③在标准状况下有2.24L气体吸收
④在标准状况下有1.12L气体吸收.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
分析 镀锌铁在发生析氢腐蚀时,较活泼的金属锌作负极,较不活泼的金属铁作正极,负极上锌失电子而被腐蚀,正极上氢离子得电子被还原,根据金属、氢气和转移电子之间的关系式计算.
解答 解:镀锌铁在发生析氢腐蚀时,较活泼的金属锌作负极,较不活泼的金属铁作正极,负极上锌失电子而被腐蚀,正极上氢离子得电子被还原.
根据Zn-2e-=Zn2+得,腐蚀锌的质量=$\frac{0.2mol}{2}$×65g/mol=6.5g;
根据2H++2e-=H2 ↑得,生成氢气的体积=$\frac{0.2mol}{2}$×22.4L/mol=2.24L,所以②④正确.
故选D.
点评 本题以金属的腐蚀为载体考查了物质的量有关计算,明确正负极上发生的反应是解本题的关键,难度不大,侧重于考查学生的分析能力和计算能力.

练习册系列答案
相关题目
14.设NA为阿伏伽德罗常数,下列关于0.2mol/L硝酸钡溶液的叙述,不正确的是( )
| A. | 2L溶液中有阴、阳离子总数为0.8NA | |
| B. | 2L溶液中硝酸根离子浓度为0.4 mol/L | |
| C. | 0.5L溶液中钡离子的浓度为0.2mol/L | |
| D. | 0.5L溶液中含有硝酸根离子的总数为0.2NA |
15.有机物 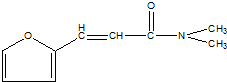 是一种高效麻醉剂,该有机物同分异构体中含有羧基(-COOH)和氨基(-NH2),且苯环上有2个取代基的有(不考虑立体异构)( )
是一种高效麻醉剂,该有机物同分异构体中含有羧基(-COOH)和氨基(-NH2),且苯环上有2个取代基的有(不考虑立体异构)( )
 是一种高效麻醉剂,该有机物同分异构体中含有羧基(-COOH)和氨基(-NH2),且苯环上有2个取代基的有(不考虑立体异构)( )
是一种高效麻醉剂,该有机物同分异构体中含有羧基(-COOH)和氨基(-NH2),且苯环上有2个取代基的有(不考虑立体异构)( )| A. | 12种 | B. | 15种 | C. | 18种 | D. | 21种 |
12.某溶液中存在较多的 Na+、SO42-、OH-,该溶液中还可能大量共存的离子是( )
| A. | H+ | B. | Ba2+ | C. | HCO3- | D. | K+ |
16.下列各组中的反应,属于同一反应类型的是( )
| A. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | |
| B. | 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 | |
| C. | 由氯代环己烷消去制环己烯;由丙烯加溴制1,2二溴丙烷 | |
| D. | 由乙酸和乙醇制乙酸乙酯;由乙酸乙酯酯水解得乙酸和乙醇 |
13.有机物C8H5O3Br的同分异构体中,苯环上含有3个取代基能与NaHCO3溶液反应且能发生银镜反应的结构共有( )(不考虑立体异构体)
| A. | 8种 | B. | 10种 | C. | 11种 | D. | 13种 |
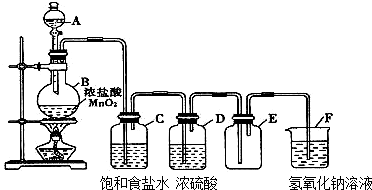
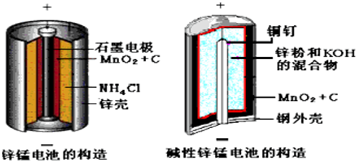



 +2H2O.
+2H2O.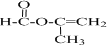 .
.