题目内容
 (1)已知:N2(g)+O2(g)═2NO(g)△H1
(1)已知:N2(g)+O2(g)═2NO(g)△H1N2(g)+3H2(g)?2NH3(g)△H2
2H2(g)+O2(g)═2H2O(g)△H3
则4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=
(2)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ?mol-1,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2O的平衡转化率的是
A.升高温度 B.增加碳的用量 C.加入催化剂 D.用CO吸收剂除去CO
(3)将一定量的CO(g)和H2O(g)分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
| 温度/℃ | 起始量/mol | 平衡量/mol[学科 | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO | ||
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
(4)工业生产是把水煤气中的混合气体经过处理后获得的较纯H2用于合成氨.合成氨反应原理为:N2(g)+3H2(g)
| 一定条件 |
请回答下列问题:
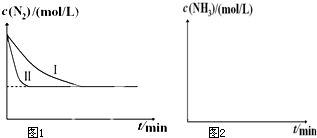
①与实验Ⅰ比较,实验Ⅱ改变的条件为
②实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在图2中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图.
考点:用盖斯定律进行有关反应热的计算,化学平衡的影响因素,化学平衡的计算
专题:化学反应中的能量变化,化学平衡专题
分析:(1)依据热化学方程式和盖斯定律计算得到所需热化学方程式;
(2)该反应是一个反应前后气体体积增大的吸热反应,升高温度、减小压强、减少生成物的量都能使平衡向正反应方向移动增大水蒸气的转化率;
(3)根据三段式计算平衡时各组分的物质的量,反应前后气体的体积不变,用物质的量代替浓度代入平衡常数表达式k=
计算;
(4)①由图开始,实验Ⅱ与实验Ⅰ相比,反应速率加快,平衡时氮气的浓度不变,说明改变条件速率加快平衡不移动,结合反应特征与平衡移动原理分析;
②实验Ⅲ的温度比实验Ⅰ高,反应速率快,到达平衡时间缩短,正反应为放热反应,平衡向逆反应方向移动,平衡时氨气的浓度较实验Ⅰ低,据此作图.
(2)该反应是一个反应前后气体体积增大的吸热反应,升高温度、减小压强、减少生成物的量都能使平衡向正反应方向移动增大水蒸气的转化率;
(3)根据三段式计算平衡时各组分的物质的量,反应前后气体的体积不变,用物质的量代替浓度代入平衡常数表达式k=
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
(4)①由图开始,实验Ⅱ与实验Ⅰ相比,反应速率加快,平衡时氮气的浓度不变,说明改变条件速率加快平衡不移动,结合反应特征与平衡移动原理分析;
②实验Ⅲ的温度比实验Ⅰ高,反应速率快,到达平衡时间缩短,正反应为放热反应,平衡向逆反应方向移动,平衡时氨气的浓度较实验Ⅰ低,据此作图.
解答:
解:(1)已知:①N2(g)+O2(g)═2NO(g)△H1
②N2(g)+3H2(g)?2NH3(g)△H2
③2H2(g)+O2(g)═2H2O(g)△H3
依据盖斯定律3×③-①×2-②×2得到热化学方程式为:4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=(3△H3-2△H1-2△H2)KJ/mol;
故答案为:3△H3-2△H1-2△H2 ;
(2)有利于提高H2O的平衡转化率,应使平衡向正反应方向移动,且不能增大水的浓度,
A.正反应为吸热反应,升高温度,平衡向正反应方向移动,水的转化率增大,故A正确;
B.碳为固体,增加碳的用量,不影响平衡移动,水的转化率不变,故B错误;
C.加入催化剂,加快反应速率,缩短到达平衡的时间,不影响平衡移动,水的转化率不变,故C错误;
D.用CO吸收剂除去CO,CO的浓度降低,平衡向正反应方向移动,水的转化率增大,故D正确,
故答案为:AD;
(3)CO(g)+H2O(g)?CO2(g)+H2(g),
起始(mol):2 1 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):1.6 0.6 0.4 0.4
反应前后气体的体积不变,用物质的量代替浓度计算平衡常数,故k=
=
=0.17,
故答案为:0.17;
(4)①由图开始,实验Ⅱ与实验Ⅰ相比,反应速率加快,平衡时氮气的浓度不变,说明改变条件速率加快平衡不移动,该反应正反应是体积减小的放热反应,升高温度或增大压强、增大反应物浓度,可以增大反应速率,但平衡发生移动,故应是使用催化剂,
故答案为:使用催化剂;实验Ⅱ与实验Ⅰ平衡状态相同,而实验Ⅱ达到平衡所需时间短;
②实验Ⅲ的温度比实验Ⅰ高,反应速率快,到达平衡时间缩短,正反应为放热反应,平衡向逆反应方向移动,平衡时氨气的浓度较实验Ⅰ低,故图象为: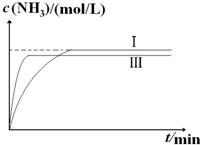 ,故答案为:
,故答案为: .
.
②N2(g)+3H2(g)?2NH3(g)△H2
③2H2(g)+O2(g)═2H2O(g)△H3
依据盖斯定律3×③-①×2-②×2得到热化学方程式为:4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=(3△H3-2△H1-2△H2)KJ/mol;
故答案为:3△H3-2△H1-2△H2 ;
(2)有利于提高H2O的平衡转化率,应使平衡向正反应方向移动,且不能增大水的浓度,
A.正反应为吸热反应,升高温度,平衡向正反应方向移动,水的转化率增大,故A正确;
B.碳为固体,增加碳的用量,不影响平衡移动,水的转化率不变,故B错误;
C.加入催化剂,加快反应速率,缩短到达平衡的时间,不影响平衡移动,水的转化率不变,故C错误;
D.用CO吸收剂除去CO,CO的浓度降低,平衡向正反应方向移动,水的转化率增大,故D正确,
故答案为:AD;
(3)CO(g)+H2O(g)?CO2(g)+H2(g),
起始(mol):2 1 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):1.6 0.6 0.4 0.4
反应前后气体的体积不变,用物质的量代替浓度计算平衡常数,故k=
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
| 0.4×0.4 |
| 1.6×0.6 |
故答案为:0.17;
(4)①由图开始,实验Ⅱ与实验Ⅰ相比,反应速率加快,平衡时氮气的浓度不变,说明改变条件速率加快平衡不移动,该反应正反应是体积减小的放热反应,升高温度或增大压强、增大反应物浓度,可以增大反应速率,但平衡发生移动,故应是使用催化剂,
故答案为:使用催化剂;实验Ⅱ与实验Ⅰ平衡状态相同,而实验Ⅱ达到平衡所需时间短;
②实验Ⅲ的温度比实验Ⅰ高,反应速率快,到达平衡时间缩短,正反应为放热反应,平衡向逆反应方向移动,平衡时氨气的浓度较实验Ⅰ低,故图象为:
 ,故答案为:
,故答案为: .
.
点评:题目综合性较大,涉及反应热计算、化学平衡图象与影响因素、化学平衡常数计算等,侧重高考常考点与基础知识的考查,目难度中等

练习册系列答案
相关题目
铅蓄电池充电时,PbSO4( )
| A、在阳极生成 |
| B、在阴极生成 |
| C、在两个电极上生成 |
| D、在两个电极上除去 |
下列关于有机物的说法错误的是( )
A、由CH2=CHCOOCH3合成的聚合物为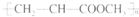 |
| B、溴乙烷与NaOH乙醇溶液共热生成乙烯 |
| C、装饰材料中的甲醛和芳香烃会造成居室污染 |
| D、磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g)?xC(g)+D(s),向甲中通入6mol A和2mol B,向乙中通入1.5mol A、0.5mol B和3mol C和2mol D,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
| A、若平衡时,甲、乙两容器中A的物质的量不相等,则x=3 |
| B、平衡时,甲、乙两容器中A、B的物质的量之比不相等 |
| C、平衡时甲中A的体积分数为40% |
| D、若平衡时两容器中的压强不相等,则两容器中压强之比为8:5 |


 ,
,