题目内容
5. 原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:(1)A、B、C三种元素第一电离能最大的是(填元素符号)N,基态E原子的电子排布式为1s22s22p63s23p63d104s2.
(2)C、D的简单氢化物中沸点较高的是H2O(填分子式),原因是水分子间存在氢键.
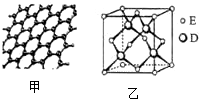
(3)A元素可形成多种单质,其中分子晶体的分子式为C60,原子晶体的名称是金刚石;A的一种单质为层状结构的晶体(如图甲),其原子的杂化轨道类型为sp2.
(4)①化合物DC2的立体构型为V形,中心原子的价层电子对数为3.
②用KMnO4酸性溶液吸收DC2气体时,MnO4-被还原为Mn2+,该反应的离子方程式为5SO2+2MnO${\;}_{4}^{-}$+2H2O═2Mn2++5SO${\;}_{4}^{2-}$+4H+.
(5)D与E能形成化合物X,X的一种晶体晶胞结构如图乙所示,X的化学式为ZnS,E的配位数为4;若晶胞边长为a,则晶体E的密度计算式为ρ=$\frac{4×97}{{a}^{3}×{N}_{A}}$.
分析 原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期,C的最外层电子数是次外层电子数的3倍,则C的最外层有6个电子,C为O元素,C与D同主族相邻,则D为S元素;A基态原子的2p轨道上有2个未成对电子,而且A的原子序数比O小,所以A为C元素;B的原子序数介于A、C之间,所以B为N元素;E位于周期表的ds区,最外层只有一对成对电子,则E为Zn元素;
(1)电子排布为半满状态,较稳定,第一电离能较大;E为Zn元素,Zn的核外有30个电子;
(2)水分子间存在氢键,氢键的作用力大于范德华力;
(3)C形成的单质中为分子晶体的是C60;属于原子晶体的是金刚石;层状结构的晶体为石墨,每个C原子形成3个共价单键,所以价层电子对数为3;
(4)①根据中心原子的价层电子对数判断;
②用KMnO4酸性溶液吸收SO2气体时,MnO4-被还原为Mn2+,根据元素守恒和电荷守恒书写;
(5)S在晶胞内部,原子数为4,Zn在顶点和面心,根据均摊法计算;晶胞中处于面心上的Zn原子与2个S原子相连,而该Zn原子被2个晶胞共用;晶胞边长为a,则晶胞的体积为a3,晶胞的质量为$\frac{4×97}{{N}_{A}}$,根据ρ=$\frac{m}{V}$计算.
解答 解:原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期,C的最外层电子数是次外层电子数的3倍,则C的最外层有6个电子,C为O元素,C与D同主族相邻,则D为S元素;A基态原子的2p轨道上有2个未成对电子,而且A的原子序数比O小,所以A为C元素;B的原子序数介于A、C之间,所以B为N元素;E位于周期表的ds区,最外层只有一对成对电子,则E为Zn元素,
(1)C、N、O三种元素中,N原子的电子排布为半满状态,较稳定,第一电离能较大,所以第一电离能最大的是N;E为Zn元素,Zn的核外有30个电子,其电子排布式为:1s22s22p63s23p63d104s2;
故答案为:N;1s22s22p63s23p63d104s2;
(2)C、D的简单氢化物分别为H2O、H2S,水分子间存在氢键,其沸点比硫化氢高;
故答案为:H2O;水分子间存在氢键;
(3)A为C元素,C形成的单质中为分子晶体的是C60;属于原子晶体的是金刚石;C的一种单质为层状结构的晶体,该单质为石墨,每个C原子形成3个共价单键,所以价层电子对数为3,其原子的杂化轨道类型为sp2;
故答案为:C60;金刚石;sp2;
(4)①化合物SO2的中S原子的价层电子对数为:2+$\frac{1}{2}$(6-2×2)=3,含有一个孤电子对,所以立体构型为V形;中心原子的价层电子对数为3;
故答案为:V形;3;
②用KMnO4酸性溶液吸收SO2气体时,MnO4-被还原为Mn2+,该反应的离子方程式为5SO2+2MnO${\;}_{4}^{-}$+2H2O═2Mn2++5SO${\;}_{4}^{2-}$+4H+;
故答案为:5SO2+2MnO${\;}_{4}^{-}$+2H2O═2Mn2++5SO${\;}_{4}^{2-}$+4H+;
(5)S与Zn形成化合物的晶胞中,S在晶胞内部,原子数为4,Zn在顶点和面心,Zn的原子数为$\frac{1}{8}$×8+$\frac{1}{2}$×6=4,所以其化学式为ZnS;晶胞中处于面心上的Zn原子与2个S原子相连,而该Zn原子被2个晶胞共用,所以配位数为4;晶胞边长为a,则晶胞的体积为a3,晶胞的质量为$\frac{4×97}{{N}_{A}}$,所以晶体E的密度为ρ=$\frac{4×97}{{a}^{3}×{N}_{A}}$;
故答案为:ZnS;4;$\frac{4×97}{{a}^{3}×{N}_{A}}$.
点评 本题考查了物质结构和性质,涉及电离能、氢键、分子结构、杂化轨道、离子方程式、晶胞结构与计算等,为常考知识点,注意掌握中学常见配合物,晶胞结构需要学生具有一定的空间想象能力,侧重对学生综合能量的考查,难度中等.

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
| A. | 青蒿素的化学式为C15H20O5 | |
| B. | 青蒿素转化为双氢青蒿素是氧化反应 | |
| C. | 青蒿素、双氢青蒿素分子内各含有2个七元环 | |
| D. | 青蒿素、双氢青蒿素分子内均含有7个手性碳原子 |
| A. | 在标准状况下1mol任何物质所占体积都是22.4升 | |
| B. | 当压强大于101KPa时1mol任何气体的体积都小于22.4升 | |
| C. | 在相同条件下,两种物质的量相同的气体必然具有相同的原子数 | |
| D. | 气体摩尔体积的数值受温度和压强的影响 |
| A. |  闻气体气味 | B. |  加热水 | C. |  倾倒液体 | D. |  移走蒸发皿 |

回答下列问题:
(1)已知:①NH3(l)═NH3(g)②N2(g)+3H2(g)═2NH3(l)△H2;则反应N2(g)+3H2(g)═2NH3(g)的△H=2△H1+△H2(用含△H1、△H2的代数式表示).
(2)合成氨的平衡常数表达式为$\frac{{c}^{3}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$,平衡时,M点NH3的体积分数为10%,则N2的转化率为18%(保留两位有效数字).
(3)X轴上a点的数值比b点小(填“大”或“小”).图中,Y轴表示温度(填“温度”或“压强”),判断的理由是随Y值增大,φ(NH3)减小,平衡N2(g)+3H2(g)?2NH3(g)△H<0向逆反应方向移动,故Y为温度.
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如表所示:
| 容器编号 | 实验条件 | 平衡时反应中的能量变化 |
| Ⅰ | 恒温恒容 | 放热Q1kJ |
| Ⅱ | 恒温恒压 | 放热Q2kJ |
| Ⅲ | 恒容绝热 | 放热Q3kJ |
A.放出热量:Ql<Q2<△Hl B.N2的转化率:Ⅰ>ⅢC.平衡常数:Ⅱ>ⅠD.达平衡时氨气的体积分数:Ⅰ>Ⅱ
(5)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)>c(S042-)(填“>”、“<”或“=”).
(6)利用氨气设计一种环保燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y203)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-.写出负极的电极反应式2NH3+3O2--6e-=N2+3H2O.
| A. | AlON和石英的化学键类型相同 | |
| B. | AlON和石英晶体类型相同 | |
| C. | AlON中N元素的化合价为-1 | |
| D. | 电解熔融AlON或电解熔融Al2O3都能得到Al |
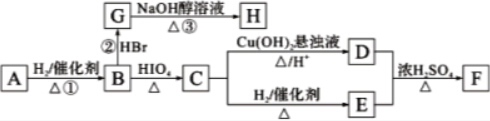
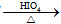 RCHO+R′CHO
RCHO+R′CHO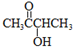 .
. CH3COO-+NH4++2Ag↓+3NH3+H2O.
CH3COO-+NH4++2Ag↓+3NH3+H2O. .若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为
.若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为 .
. .
.