题目内容
 如图表示一个电解池.X、Y都是惰性电极,电解液a是饱和食盐水,同时在两边各滴入几滴酚酞试液.
如图表示一个电解池.X、Y都是惰性电极,电解液a是饱和食盐水,同时在两边各滴入几滴酚酞试液.(1)X极上的电极反应式为
(2)Y极上的电极反应式为
考点:电解原理
专题:电化学专题
分析:电解饱和食盐水时,阳极上是氯离子失电子,阴极上是氢离子得电子,溶液中氢氧根离子浓度增大,遇到酚酞变红色;
解答:
解:(1)X和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,
故答案为:2H++2e-=H2↑或2H2O+2e-=H2+2OH-;放出气体,溶液变红;
(2)Y和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,检验氯气用湿润的淀粉碘化钾试纸,
故答案为:2Cl--2e-=Cl2↑,用湿润的淀粉碘化钾试纸变蓝,说明生成氯气;
故答案为:2H++2e-=H2↑或2H2O+2e-=H2+2OH-;放出气体,溶液变红;
(2)Y和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,检验氯气用湿润的淀粉碘化钾试纸,
故答案为:2Cl--2e-=Cl2↑,用湿润的淀粉碘化钾试纸变蓝,说明生成氯气;
点评:本题考查学生电解池的工作原理知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
下列关于化学键的说法正确的是( )
①含有金属元素的化合物一定是离子化合物 ②第ⅠA族和第ⅦA族原子化合时,一定生成离子键
③由非金属元素形成的化合物一定不是离子化合物 ④活泼金属与非金属化合时,能形成离子键
⑤含有离子键的化合物一定是离子化合物 ⑥离子化合物中可能同时含有离子键和共价键.
①含有金属元素的化合物一定是离子化合物 ②第ⅠA族和第ⅦA族原子化合时,一定生成离子键
③由非金属元素形成的化合物一定不是离子化合物 ④活泼金属与非金属化合时,能形成离子键
⑤含有离子键的化合物一定是离子化合物 ⑥离子化合物中可能同时含有离子键和共价键.
| A、①②⑤ | B、④⑤⑥ |
| C、①③④ | D、②③⑤ |
据报道,光合作用能够借助太阳能用CO2和H2制备RCH其反应原理如下:2CO2+2H2O
2HCOOH+O2,下列说法正确的是( )
| ||
| A、HCOOH分子中既有极性键,又有非极性键 |
| B、反应中,CO2被氧化,O2是还原产物 |
| C、反应中,每转移4×6.02×1023个电子,生成2.24L气体 |
| D、该过程是将太阳能转化为化学能的过程 |




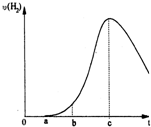 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图坐标曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图坐标曲线来表示,回答下列问题: 现有甲晶体的晶胞如图所示.甲中X处于晶胞中心由此可知:甲晶体中X与Y的个数比是
现有甲晶体的晶胞如图所示.甲中X处于晶胞中心由此可知:甲晶体中X与Y的个数比是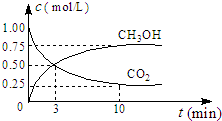 联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.