题目内容
 “低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
(2)将不同量的CO(g)和H2O(g)分别通入到体积为 2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)?CO2(g)+H2(g),得到如表二组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1451.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
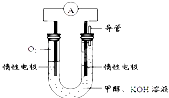
(4)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.
①该电池正极的电极反应为
②该电池工作时,溶液中的OH-向
考点:氧化还原反应方程式的配平,热化学方程式,化学电源新型电池,化学平衡的影响因素
专题:基本概念与基本理论
分析:(1)根据氧化还原反应中得失电子数相等和原子守恒来配平化学方程式;
(2)①由表中数据可知,CO的物质的量变化量为4mol-2.4mol=1.6mol,根据v=
计算v(CO),再利用速率之比等于化学计量数之比计算v(CO2);
②利用三段式计算平衡时,各组分的物质的量,该反应是气体体积不变的反应,故利用物质的量代替浓度代入平衡常数表达式计算平衡常数;第二组温度比第一组高,反应物物质的量比第一组减半,但是平衡时CO2的物质的量比第一组的一半少,表明该反应为放热反应;
(3)根据热化学方程式和盖斯定律计算进行书写;
(4)①该燃料电池中,负极反应为CH3OH-6e-+2OH-=CO32-+3H2O,正极上氧气得电子发生还原反应,电极反应为O2+2H2O+4e-=4OH-;
②溶液中的OH-向负极移动.
(2)①由表中数据可知,CO的物质的量变化量为4mol-2.4mol=1.6mol,根据v=
| △n | ||
|
②利用三段式计算平衡时,各组分的物质的量,该反应是气体体积不变的反应,故利用物质的量代替浓度代入平衡常数表达式计算平衡常数;第二组温度比第一组高,反应物物质的量比第一组减半,但是平衡时CO2的物质的量比第一组的一半少,表明该反应为放热反应;
(3)根据热化学方程式和盖斯定律计算进行书写;
(4)①该燃料电池中,负极反应为CH3OH-6e-+2OH-=CO32-+3H2O,正极上氧气得电子发生还原反应,电极反应为O2+2H2O+4e-=4OH-;
②溶液中的OH-向负极移动.
解答:
解:(1)高锰酸钾中锰元素化合价降低7-2=5价,碳元素化合价升高4-0=4价,化合价升高数=化合价降低数,所以高锰酸钾前的系数是4,碳单质前的系数是5,根据原子守恒,二氧化碳前是5,硫酸锰前是4,硫酸钾前面是2,根据硫酸跟守恒,所以硫酸前面是6,据氧原子和氢原子守恒,产物少6个水分子,
故答案为:5;4;6;5;4;2;6H2O;
(2)①由表中数据可知,CO的物质的量变化量为4mol-2.4mol=1.6mol,v(CO)=
=
=
mol/(L?min),速率之比等于化学计量数之比,故v(CO2)=v(CO)=
mol/(L?min)=0.13mol/(L?min),故答案为:0.13mol/(L?min);
②平衡时CO的物质的量为1.6mol,则:
CO(g)+H2O(g)?CO2(g)+H2(g),
开始(mol):2 1 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):1.6 0.6 0.4 0.4
该反应前后气体体积不变,故利用物质的量代替浓度计算平衡常数,故900℃时该反应平衡常数k=
=0.17,实验1中CO的转化率为×100%=40%,实验2中CO的转化率为×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热,
故答案为:0.17;放热;
(3)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1451.6kJ/mol
②2CO (g)+O2(g)=2CO2 (g)△H2=-566.0kJ/mol
根据盖斯定律,①-②得2CH3OH(l)+2O2(g)=2CO(g)+4H2O(l),该反应的反应热△H=-1451.6kJ/mol
-(-566.0kJ/mol)=-885.6kJ/mol
故该反应热化学方程式为:CH3OH(l)+O2(g)=CO(g)+2 H2O(l)△H=-442.8kJ/mol,
故答案为:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol;
(4)①该燃料电池中,正极上氧气得电子和水生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,故答案为:O2+2H2O+4e-=4OH-;
②溶液中的OH-向负极移动,故答案为:负.
故答案为:5;4;6;5;4;2;6H2O;
(2)①由表中数据可知,CO的物质的量变化量为4mol-2.4mol=1.6mol,v(CO)=
| △n | ||
|
| 1.6mol | ||
|
| 2 |
| 15 |
| 2 |
| 15 |
②平衡时CO的物质的量为1.6mol,则:
CO(g)+H2O(g)?CO2(g)+H2(g),
开始(mol):2 1 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):1.6 0.6 0.4 0.4
该反应前后气体体积不变,故利用物质的量代替浓度计算平衡常数,故900℃时该反应平衡常数k=
| 0.4×0.4 |
| 1.6×0.6 |
故答案为:0.17;放热;
(3)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1451.6kJ/mol
②2CO (g)+O2(g)=2CO2 (g)△H2=-566.0kJ/mol
根据盖斯定律,①-②得2CH3OH(l)+2O2(g)=2CO(g)+4H2O(l),该反应的反应热△H=-1451.6kJ/mol
-(-566.0kJ/mol)=-885.6kJ/mol
故该反应热化学方程式为:CH3OH(l)+O2(g)=CO(g)+2 H2O(l)△H=-442.8kJ/mol,
故答案为:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol;
(4)①该燃料电池中,正极上氧气得电子和水生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,故答案为:O2+2H2O+4e-=4OH-;
②溶液中的OH-向负极移动,故答案为:负.
点评:本题考查较为综合,涉及化学平衡常数、化学平衡计算、热化学方程式书写、原电池等,题目难度中等.难点是电极反应式的书写,要注意结合电解质溶液酸碱性书写.

练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
在水中加入下列物质,可以促进水电离的是( )
| A、H2SO4 |
| B、NaOH |
| C、KNO3 |
| D、Na2CO3 |
下列说法错误的是( )
| A、“血液透析”利用了胶体的性质 |
| B、向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 |
| C、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| D、依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
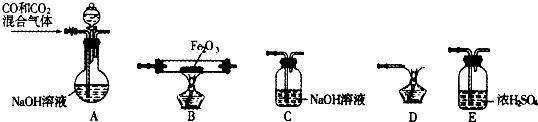

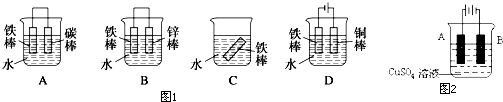
 人胃酸过多会引起很多胃病.如图为某抗酸药包装标签上的部分文字,某同学欲检验该抗酸药有效成分是否是Al(OH)3,并测定该药片中氢氧化铝的含量是否达到标签标注的含量.请回答下列问题.
人胃酸过多会引起很多胃病.如图为某抗酸药包装标签上的部分文字,某同学欲检验该抗酸药有效成分是否是Al(OH)3,并测定该药片中氢氧化铝的含量是否达到标签标注的含量.请回答下列问题.