题目内容
铁工业是国家工业的基础,请回答钢铁腐蚀与防护过程中的有关问题.
(1)生产中可用盐酸来除铁锈.现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化学反应的化学方程式是 .
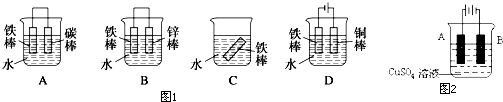
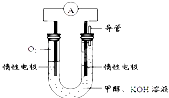
(2)图1哪个装置可防止铁棒被腐蚀 .
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如下:
①A电极对应的金属是 (写元素名称),B电极的电极反应式是 .
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为 mol.
③下列说法正确的是 .
a.此装置实现了化学能转化为电能
b.镀层破损后,镀铜铁比镀锌铁更容易被腐蚀
c.溶液中Cu2+浓度保持不变
d.A极可用碳棒代替金属.

(1)生产中可用盐酸来除铁锈.现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化学反应的化学方程式是
(2)图1哪个装置可防止铁棒被腐蚀
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如下:
①A电极对应的金属是
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为
③下列说法正确的是
a.此装置实现了化学能转化为电能
b.镀层破损后,镀铜铁比镀锌铁更容易被腐蚀
c.溶液中Cu2+浓度保持不变
d.A极可用碳棒代替金属.
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:(1)氧化铁可以和盐酸之间反应生成氯化铁和水,金属铁可以和盐酸反应得到氢气,金属铁也可以和氯化铁之间反应得到氯化亚铁;
(2)根据金属生锈的条件以及原电池和电解池的工作原理知识来回答判断;
(3)①电镀时,镀层作阳极,镀件作阴极;
②电镀时,阳极上金属失电子导致金属质量减少,阴极上析出金属,导致质量增加,电镀后两极质量差的一半为阴极上析出的铜质量,根据析出铜质量和转移电子之间的关系式计算;
③a、电镀是电能转化为化学能;
b、据原电池原理分析;
c、据电镀原理解和阳极材料分析;
d、据电镀原理分析.
(2)根据金属生锈的条件以及原电池和电解池的工作原理知识来回答判断;
(3)①电镀时,镀层作阳极,镀件作阴极;
②电镀时,阳极上金属失电子导致金属质量减少,阴极上析出金属,导致质量增加,电镀后两极质量差的一半为阴极上析出的铜质量,根据析出铜质量和转移电子之间的关系式计算;
③a、电镀是电能转化为化学能;
b、据原电池原理分析;
c、据电镀原理解和阳极材料分析;
d、据电镀原理分析.
解答:
解:(1)氧化铁可以和盐酸之间反应生成氯化铁和水,当铁锈除净后,金属铁可以和盐酸反应得到氢气,金属铁也可以和氯化铁之间反应得到氯化亚铁,即Fe+2HCl=FeCl2+H2↑,2FeCl3+Fe=3FeCl2,
故答案为:Fe+2HCl=FeCl2+H2↑;2FeCl3+Fe=3FeCl2;
(2)B装置中,金属铁做原电池的正极,被保护,不易生锈,D装置中,金属铁作阴极,被保护起来,C装置具备金属生锈的条件,A装置中,金属铁是原电池的负极,易被腐蚀,
故答案为:BD;
(3)①在铁上镀铜时,铜作阳极连接原电池正极,铁作阴极连接原电池负极,所以A为铜,B为铁,铁电极上铜离子得电子生成铜单质,
电极反应式为 Cu2++2e-═Cu,
故答案为:铜;Cu2++2e-═Cu;
②电镀时,阳极上金属失电子导致金属质量减少,阴极上析出金属,导致质量增加,电镀后两极质量差的一半为阴极上析出的铜质量,
所以阴极上析出铜的质量=5.12g×
=2.56g,转移电子的物质的量=
=0.08 mol,
故答案为:0.08;
③a、电镀是电能转化为化学能,故a错误;
b、铁比铜活泼,锌比铁活泼,活泼金属做负极,腐蚀快,故b正确;
c、电镀过程中溶液中铜离子损耗速度与阳极上生成速度相等,故c正确;
d、A极用碳棒代替后,溶液中的铜离子在阴极得电子,照样实现电镀,故d正确;
故选bcd.
故答案为:Fe+2HCl=FeCl2+H2↑;2FeCl3+Fe=3FeCl2;
(2)B装置中,金属铁做原电池的正极,被保护,不易生锈,D装置中,金属铁作阴极,被保护起来,C装置具备金属生锈的条件,A装置中,金属铁是原电池的负极,易被腐蚀,
故答案为:BD;
(3)①在铁上镀铜时,铜作阳极连接原电池正极,铁作阴极连接原电池负极,所以A为铜,B为铁,铁电极上铜离子得电子生成铜单质,
电极反应式为 Cu2++2e-═Cu,
故答案为:铜;Cu2++2e-═Cu;
②电镀时,阳极上金属失电子导致金属质量减少,阴极上析出金属,导致质量增加,电镀后两极质量差的一半为阴极上析出的铜质量,
所以阴极上析出铜的质量=5.12g×
| 1 |
| 2 |
| 2.56g |
| 64g/mol |
故答案为:0.08;
③a、电镀是电能转化为化学能,故a错误;
b、铁比铜活泼,锌比铁活泼,活泼金属做负极,腐蚀快,故b正确;
c、电镀过程中溶液中铜离子损耗速度与阳极上生成速度相等,故c正确;
d、A极用碳棒代替后,溶液中的铜离子在阴极得电子,照样实现电镀,故d正确;
故选bcd.
点评:本题考查原电池和电解池的工作原理以及金属的腐蚀和防护知识,注意知识的归纳和整理是解题关键,根据电镀原理、金属的腐蚀与防护来分析解答即可,题目难度中等.

练习册系列答案
相关题目
下列化学用语中,书写错误的是( )
A、硫离子的结构示意图: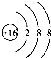 |
| B、次氯酸的结构式:H-O-Cl |
C、CO2的比例模型: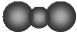 |
D、丙烷的球棍模型: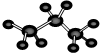 |
下列关于Al(OH)3的性质叙述中错误的是( )
| A、Al(OH)3与过量的浓氨水反应生成NH4AlO2 |
| B、Al(OH)3是难溶于水的白色胶状物质 |
| C、Al(OH)3胶体能凝聚水中的悬浮物 |
| D、Al(OH)3受热能分解 |
下列各组反应中最终肯定不生成白色沉淀的是( )
| A、AlCl3溶液中加入过量的氨水 |
| B、MgCl2溶液中加入过量的氨水 |
| C、Al2(SO4)3溶液中加入过量的KOH溶液 |
| D、MgSO4溶液中加入过量的KOH溶液 |
下列各组离子能大量共存的是( )
| A、I-、ClO-、H+、Na+ |
| B、K+、HCO3-、OH-、NH4+ |
| C、Fe3+、Cu2+、SO42-、Cl- |
| D、Ca2+、Na+、SO42-、SO32- |
元素周期表和元素周期律的有关说法,正确的是( )
| A、元素周期表第8、9、10三纵列合称Ⅷ族,Ⅷ族是元素周期表所有族中元素种类最多的族 |
| B、元素周期表中的所有副族元素都是金属元素,副族包含过渡元素和Ⅷ族 |
| C、在同一主族中,从上到下,F、Cl、Br、I的非金属性逐渐减弱 |
| D、因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S |
 “低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.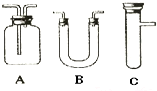 浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C
浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C