题目内容
化学实验在化学学习中具有重要的作用.
(1)下列与实验有关的叙述正确的是 (填序号).
①氨水、浓硝酸和溴化银都必须存放在配有磨口塞的棕色玻璃瓶中
②容量瓶、分液漏斗、酸(碱)式滴定管等仪器在使用前都必须检验是否漏水
③用稀盐酸即可鉴别Na2SiO3、NaHCO3、Na[Al(OH)4]、Na2SO4四种溶液
④乙酸与乙醇的混合液可用分液漏斗进行分离
⑤用托盘天平准确称取29.25gNaCl固体,配制500mL 0.5mol?L-1 NaCl溶液
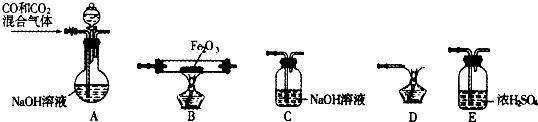
(2)实验室用Fe2O3与CO反应来制取单质Fe.
①请按气流方向连接下列所有装置(每种装置只允许使用一次),合理的顺序为A→ .
②装置C的作用是 .

(1)下列与实验有关的叙述正确的是
①氨水、浓硝酸和溴化银都必须存放在配有磨口塞的棕色玻璃瓶中
②容量瓶、分液漏斗、酸(碱)式滴定管等仪器在使用前都必须检验是否漏水
③用稀盐酸即可鉴别Na2SiO3、NaHCO3、Na[Al(OH)4]、Na2SO4四种溶液
④乙酸与乙醇的混合液可用分液漏斗进行分离
⑤用托盘天平准确称取29.25gNaCl固体,配制500mL 0.5mol?L-1 NaCl溶液
(2)实验室用Fe2O3与CO反应来制取单质Fe.
①请按气流方向连接下列所有装置(每种装置只允许使用一次),合理的顺序为A→
②装置C的作用是
考点:实验装置综合,化学实验方案的评价
专题:实验设计题,实验评价题
分析:(1)①碱性溶液不能用配有磨口塞的玻璃瓶盛放;
②带有活塞和玻璃塞的仪器使用前都必须检验是否漏水;
③根据反应的现象判断,现象各不相同即可鉴别;
④分液漏斗用于分离互不相溶的液体;
⑤托盘天平的精确度为0.1g;
(2)①根据实验目的和实验原理进行分析,本实验的目的为用Fe2O3与CO反应来制取单质Fe,用除去二氧化碳和水蒸气;
②氢氧化钠溶液能吸收CO2.
②带有活塞和玻璃塞的仪器使用前都必须检验是否漏水;
③根据反应的现象判断,现象各不相同即可鉴别;
④分液漏斗用于分离互不相溶的液体;
⑤托盘天平的精确度为0.1g;
(2)①根据实验目的和实验原理进行分析,本实验的目的为用Fe2O3与CO反应来制取单质Fe,用除去二氧化碳和水蒸气;
②氢氧化钠溶液能吸收CO2.
解答:
解:(1)①碱性溶液不能用配有磨口塞的玻璃瓶盛放,所以氨水不能存放在配有磨口塞的棕色玻璃瓶中,故错误;
②带有活塞和玻璃塞的仪器使用前都必须检验是否漏水,所以容量瓶、分液漏斗、酸(碱)式滴定管等仪器在使用前都必须检验是否漏水,故正确;
③将稀盐酸分别滴入Na2SiO3、NaHCO3、Na[Al(OH)4]、Na2SO4四种溶液中,产生的现象分别为产生白色沉淀、产生气体、先产生白色沉淀后消失、无现象,现象各不相同,可以鉴别,故正确;
④乙酸与乙醇互溶,不能用分液漏斗进行分离,应用蒸馏法分离,故错误;
⑤托盘天平的精确度为0.1g,不能用托盘天平准确称取29.25gNaCl固体,故错误;
故答案为:②③;
(2)实验的目的是用Fe2O3与CO反应来制取单质Fe,分析题给装置知,A装置CO和CO2的混合气体通过NaOH溶液,CO2被吸收,可提供还原剂CO,但CO中含有水蒸气,Fe2O3与CO反应需要加热,所以先通过E装置中的浓硫酸除去水蒸气,CO气体有毒,必须进行尾气处理,用点燃的方法,选D装置,但氧化产物CO2的存在,影响CO的点燃,必须先用C装置中的氢氧化钠溶液除去尾气中CO2,所以合理的顺序为A→E→B→C→D;
故答案为:E→B→C→D;
②氢氧化钠溶液能吸收CO2,则装置C的作用是除去CO中的CO2,有利于点燃CO,故答案为:除去CO中的CO2,有利于点燃CO.
②带有活塞和玻璃塞的仪器使用前都必须检验是否漏水,所以容量瓶、分液漏斗、酸(碱)式滴定管等仪器在使用前都必须检验是否漏水,故正确;
③将稀盐酸分别滴入Na2SiO3、NaHCO3、Na[Al(OH)4]、Na2SO4四种溶液中,产生的现象分别为产生白色沉淀、产生气体、先产生白色沉淀后消失、无现象,现象各不相同,可以鉴别,故正确;
④乙酸与乙醇互溶,不能用分液漏斗进行分离,应用蒸馏法分离,故错误;
⑤托盘天平的精确度为0.1g,不能用托盘天平准确称取29.25gNaCl固体,故错误;
故答案为:②③;
(2)实验的目的是用Fe2O3与CO反应来制取单质Fe,分析题给装置知,A装置CO和CO2的混合气体通过NaOH溶液,CO2被吸收,可提供还原剂CO,但CO中含有水蒸气,Fe2O3与CO反应需要加热,所以先通过E装置中的浓硫酸除去水蒸气,CO气体有毒,必须进行尾气处理,用点燃的方法,选D装置,但氧化产物CO2的存在,影响CO的点燃,必须先用C装置中的氢氧化钠溶液除去尾气中CO2,所以合理的顺序为A→E→B→C→D;
故答案为:E→B→C→D;
②氢氧化钠溶液能吸收CO2,则装置C的作用是除去CO中的CO2,有利于点燃CO,故答案为:除去CO中的CO2,有利于点燃CO.
点评:本题考查了实验方案设计,侧重于考查学生的实验探究能力,题目涉及了试剂的保存、仪器的使用、物质的鉴别、实验原理的分析等,题目难度中等.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
甲、乙两烧杯中各盛有100mL 3mol/L盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为3:4,则加入铝粉的质量为( )
| A、5.4g | B、3.6g |
| C、2.7g | D、1.6g |
同温同压下,下列关于氢气和氧气的叙述中,错误的是( )
| A、等体积的氢气和氧气所含的分子数相等 |
| B、氢分子与氧分子大小相同 |
| C、氢分子间的平均距离和氧分子间的平均距离几乎是相等的 |
| D、氢分子和氧分子本身的大小对于气体体积影响可以忽略不计 |
下列关于Al(OH)3的性质叙述中错误的是( )
| A、Al(OH)3与过量的浓氨水反应生成NH4AlO2 |
| B、Al(OH)3是难溶于水的白色胶状物质 |
| C、Al(OH)3胶体能凝聚水中的悬浮物 |
| D、Al(OH)3受热能分解 |
在室温时,下列各组中的物质分别与过量NaOH溶液反应,能生成5种盐的是( )
| A、MgO、Al2O3、SO2、CO2 |
| B、CO2、Cl2、CaO、SO3 |
| C、Cl2、Al2O3、N2O3、SO3 |
| D、SiO2、N2O5、CO、Cl2 |
下列各组反应中最终肯定不生成白色沉淀的是( )
| A、AlCl3溶液中加入过量的氨水 |
| B、MgCl2溶液中加入过量的氨水 |
| C、Al2(SO4)3溶液中加入过量的KOH溶液 |
| D、MgSO4溶液中加入过量的KOH溶液 |
元素周期表和元素周期律的有关说法,正确的是( )
| A、元素周期表第8、9、10三纵列合称Ⅷ族,Ⅷ族是元素周期表所有族中元素种类最多的族 |
| B、元素周期表中的所有副族元素都是金属元素,副族包含过渡元素和Ⅷ族 |
| C、在同一主族中,从上到下,F、Cl、Br、I的非金属性逐渐减弱 |
| D、因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S |
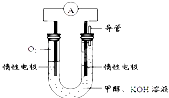 “低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.
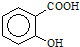 )可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式
)可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式