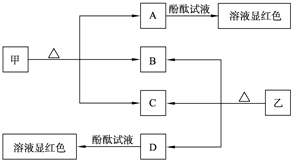
题目内容
KMnO4是一种重要的氧化剂.
(1)①在酸性条件下KMnO4的氧化性会增强.用来酸化KMnO4溶液的最佳试剂是 .
a.硝酸 b.硫酸 c.盐酸
②将MnO4-氧化C2O42-的离子方程式补充完整:
MnO4-+ C2O42-+ ═ Mn2++ CO2↑+ .
(2)某同学为了探究KMnO4溶液和Na2C2O4(草酸钠)溶液的反应过程,进行如下实验:
①配制100mL 0.0400mol?L-1的Na2C2O4溶液,除用到托盘天平、药匙、烧杯、量筒、玻璃棒等仪器外,还必须用到的玻璃仪器是 .
②将KMnO4溶液逐滴滴入一定体积的酸性Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如表:
请分析KMnO4溶液褪色时间变化的可能原因 .
③用配制好的0.040 0mol?L-1的Na2C2O4溶液来标定某KMnO4溶液的浓度.每次准确量取25.00mLNa2C2O4溶液,然后用酸化后的KMnO4溶液滴定.滴定三次分别消耗的KMnO4溶液的体积是20.00mL、19.80mL、20.20mL,则KMnO4溶液的浓度为 .
(1)①在酸性条件下KMnO4的氧化性会增强.用来酸化KMnO4溶液的最佳试剂是
a.硝酸 b.硫酸 c.盐酸
②将MnO4-氧化C2O42-的离子方程式补充完整:
(2)某同学为了探究KMnO4溶液和Na2C2O4(草酸钠)溶液的反应过程,进行如下实验:
①配制100mL 0.0400mol?L-1的Na2C2O4溶液,除用到托盘天平、药匙、烧杯、量筒、玻璃棒等仪器外,还必须用到的玻璃仪器是
②将KMnO4溶液逐滴滴入一定体积的酸性Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如表:
| 滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 | 60s |
| 褪色后,再滴入第2滴 | 15s |
| 褪色后,再滴入第3滴 | 3s |
| 褪色后,再滴入第4滴 | 1s |
③用配制好的0.040 0mol?L-1的Na2C2O4溶液来标定某KMnO4溶液的浓度.每次准确量取25.00mLNa2C2O4溶液,然后用酸化后的KMnO4溶液滴定.滴定三次分别消耗的KMnO4溶液的体积是20.00mL、19.80mL、20.20mL,则KMnO4溶液的浓度为
考点:氧化还原反应方程式的配平,化学方程式的有关计算
专题:氧化还原反应专题
分析:(1)①高锰酸钾能氧化盐酸,硝酸本身具有强氧化性,故选硫酸;
②草酸根离子具有还原性,把MnO4-还原为Mn2+,根据化合价升降方法,反应中MnO4-→Mn2+,锰元素化合价由+7价降低为+2价,共降低5价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为10,故MnO4-系数为2,C2O42-系数为5,再根据元素守恒、电荷守恒确定其它物质的系数;
(2)①根据配制溶液的步骤和所用仪器即可判断;
②反应中Mn2+浓度发生显著变化,应是反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好;
③令KMnO4溶液的浓度为c,根据方程式2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O计算;
②草酸根离子具有还原性,把MnO4-还原为Mn2+,根据化合价升降方法,反应中MnO4-→Mn2+,锰元素化合价由+7价降低为+2价,共降低5价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为10,故MnO4-系数为2,C2O42-系数为5,再根据元素守恒、电荷守恒确定其它物质的系数;
(2)①根据配制溶液的步骤和所用仪器即可判断;
②反应中Mn2+浓度发生显著变化,应是反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好;
③令KMnO4溶液的浓度为c,根据方程式2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O计算;
解答:
解:(1)①高锰酸钾能氧化盐酸,硝酸本身具有强氧化性,故选硫酸,
故答案为:b;
②反应中MnO4-→Mn2+,锰元素化合价由+7价降低为+2价,共降低5价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为10,故MnO4-系数为2,C2O42-系数为5,再根据元素守恒可知Mn2+系数为2、CO2系数为10,根据电荷守恒可知H+系数为16,根据氢元素守恒可知H2O系数为8,配平后离子方程式为2MnO4-+5C2O42-+16H+=2Mn2++10CO2+8H2O,
故答案为:2;5;16H+;2;10;8H2O;
(2)①配制100mL 0.0400mol?L-1的Na2C2O4溶液,配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到100mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、量筒、药匙、烧杯、玻璃棒、100mL容量瓶、胶头滴管,该试验中两次用到玻璃棒,其作用分别是搅拌、引流,所以还必须用到的玻璃仪器是100mL容量瓶、胶头滴管,
故答案为:100mL容量瓶、胶头滴管;
②反应中Mn2+浓度发生显著变化,应是反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好,
故答案为:反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好;
③滴定三次分别消耗的KMnO4溶液的体积是20.00mL、19.80mL、20.20mL,消耗的KMnO4溶液的体积平均为是
=20mL,
n(C2O42-)=
=0.01mol,则:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
2mol 5mol
c×0.02L×10 0.01mol
所以2mol:5mol=c×0.02L×10:0.01mol,
解得c=0.02mol/L,
故答案为:0.02mol/L.
故答案为:b;
②反应中MnO4-→Mn2+,锰元素化合价由+7价降低为+2价,共降低5价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为10,故MnO4-系数为2,C2O42-系数为5,再根据元素守恒可知Mn2+系数为2、CO2系数为10,根据电荷守恒可知H+系数为16,根据氢元素守恒可知H2O系数为8,配平后离子方程式为2MnO4-+5C2O42-+16H+=2Mn2++10CO2+8H2O,
故答案为:2;5;16H+;2;10;8H2O;
(2)①配制100mL 0.0400mol?L-1的Na2C2O4溶液,配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到100mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、量筒、药匙、烧杯、玻璃棒、100mL容量瓶、胶头滴管,该试验中两次用到玻璃棒,其作用分别是搅拌、引流,所以还必须用到的玻璃仪器是100mL容量瓶、胶头滴管,
故答案为:100mL容量瓶、胶头滴管;
②反应中Mn2+浓度发生显著变化,应是反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好,
故答案为:反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好;
③滴定三次分别消耗的KMnO4溶液的体积是20.00mL、19.80mL、20.20mL,消耗的KMnO4溶液的体积平均为是
| 20.00mL+19.80mL+20.20mL |
| 3 |
n(C2O42-)=
| 1.34g |
| 134g/mol |
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
2mol 5mol
c×0.02L×10 0.01mol
所以2mol:5mol=c×0.02L×10:0.01mol,
解得c=0.02mol/L,
故答案为:0.02mol/L.
点评:本题考查溶液的配制、氧化还原反应配平、氧化还原反应滴定应用、化学计算等,难度中等,注意把握实验的原理,需要学生具备一定的理论分析能力和计算解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组反应中能得到Al(OH)3的是( )
| A、Al2O3加到热水中 |
| B、向NaAlO2溶液中加入过量盐酸 |
| C、将Na投入到NaAlO2溶液中 |
| D、在AlCl3溶液中滴几滴NaOH溶液 |
靛青是一种染料,利用元素分析仪分析其样品,发现它只含碳、氢、氧、氮四种元素,四种元素的质量分数分别如下:碳为73.3%、氢为3.8%、氮为10.7%、氧为12.2%.则靛青的最简式为( )
| A、C8H5NO |
| B、C2H2NO |
| C、C4H6NO |
| D、C7H8NO |
将等体积的Na2S溶液和Na2SO3溶液混合,并加入适量的稀硫酸,产生黄色沉淀,微热,无酸性气体放出,则原混合液中Na2S和Na2SO3的物质的量之比为( )
| A、3:2 | B、2:1 |
| C、1:2 | D、1:1 |
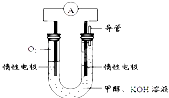 “低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.
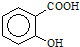 )可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式
)可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式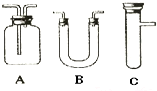 浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C
浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C