题目内容
下列日常生活中的现象与氧化还原反应无关的是( )
| A、铜铸塑像上出现铜绿[Cu2(0H)2C03] |
| B、用石膏点豆腐 |
| C、不良商贩用硫黄熏蒸法制作“白豆芽” |
| D、自来水厂用氯气对水进行消毒 |
考点:氧化还原反应
专题:
分析:生活现象中涉及的化学反应中,若有元素的化合价变化,则反应为氧化还原反应,以此来解答.
解答:
解:A.铜铸塑像上出现铜绿[Cu2(0H)2C03],变化过程中Cu元素的化合价从0价升高到+2价,与氧化还原反应有关,故A不选;
B.用石膏点豆腐,是利用了胶体聚沉的性质,没有元素化合价的变化,不是氧化还原反应,故B选;
C.不良商贩用硫黄熏蒸法制作“白豆芽”,S与氧气反应生成二氧化硫,S、O的化合价发生变化,与氧化还原反应有关,故C不选;
D.自来水厂用氯气对水进行消毒,氯气与水反应生成HCl和HClO,Cl元素的化合价发生变化,是氧化还原反应,故D不选;
故选B.
B.用石膏点豆腐,是利用了胶体聚沉的性质,没有元素化合价的变化,不是氧化还原反应,故B选;
C.不良商贩用硫黄熏蒸法制作“白豆芽”,S与氧气反应生成二氧化硫,S、O的化合价发生变化,与氧化还原反应有关,故C不选;
D.自来水厂用氯气对水进行消毒,氯气与水反应生成HCl和HClO,Cl元素的化合价发生变化,是氧化还原反应,故D不选;
故选B.
点评:本题考查氧化还原反应,把握反应中的元素化合价变化为解答的关键,侧重氧化还原反应判断与生活中化学的联系的考查,题目难度不大.

练习册系列答案
相关题目
24mL浓度为0.05mol?L-1的Na2SO3溶液,恰好与20mL浓度为0.02mol?L-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为( )
| A、+2 | B、+3 | C、+4 | D、+5 |
下列指定反应的离子方程式正确的是( )
| A、NaHCO3溶液中加入醋酸溶液:HCO3-+H+=CO2↑+H2O | ||
| B、NaAlO2溶液中通入过量CO2气体:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- | ||
| C、Fe(OH)2溶于足量稀硝酸:Fe(OH)2+2H+=Fe2++2H2O | ||
D、乙醛与含有NaOH的Cu(OH)2悬浊液共热:CH3CHO+OH-+2Cu(OH)2
|
酸性条件下20mL、0.5mol/L的 KMnO4溶液可将25mL、2mol/L的FeSO4溶液中的 Fe2+氧化为Fe3+,则KMnO4被还原的产物是( )
| A、Mn2O3 |
| B、Mn2+ |
| C、MnO2 |
| D、K2MnO4 |
实验室需配制一种仅含四种离子(不考虑水的电离)的混合溶液,且在混合溶液中四种离子的物质的量浓度均为0.1mol/L.下面四个选项中能达到此目的是( )
| A、Na+、K+、SO42-、Cl- |
| B、Fe2+、H+、SO42-、NO3- |
| C、H+、K+、HCO3-、Cl- |
| D、Mg2+、Na+、Cl-、SO42- |
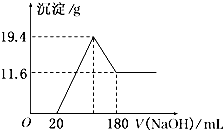 将可能含有少量碳、硅杂质的a克镁铝合金投入100mL一定物质的量浓度的盐酸中,合金部分溶解,过滤,向所得溶液中滴加5mol/L NaOH溶液至过量,生成沉淀的质量与加入氢氧化钠溶液的体积的关系如图所示.
将可能含有少量碳、硅杂质的a克镁铝合金投入100mL一定物质的量浓度的盐酸中,合金部分溶解,过滤,向所得溶液中滴加5mol/L NaOH溶液至过量,生成沉淀的质量与加入氢氧化钠溶液的体积的关系如图所示.