题目内容
10.6gNa2CO3与足量盐酸完全反应,生成CO2的质量是多少?需要HCl的物质的量是多少?
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O,根据n=
计算10.6g Na2CO3 的物质的量,根据方程式计算生成的二氧化碳的物质的量、参加反应n(HCl),根据m=nM计算生成的二氧化碳的质量,根据c=
计算盐酸的物质的量浓度.
| m |
| M |
| n |
| V |
解答:
解:10.6g Na2CO3 的物质的量为
=0.1mol,则:
Na2CO3+2HCl=2NaCl+CO2↑+H2O
1 2 1
0.1mol n(HCl) n(CO2)
所以n(HCl)=0.1mol×2=0.2mol,n(CO2)=0.1mol,
二氧化碳的质量=0.1mol×44g/mol=4.4g,
答:产生的CO2的质量为4.4g,需要HCl的物质的量为0.2mol.
| 10.6g |
| 106g/mol |
Na2CO3+2HCl=2NaCl+CO2↑+H2O
1 2 1
0.1mol n(HCl) n(CO2)
所以n(HCl)=0.1mol×2=0.2mol,n(CO2)=0.1mol,
二氧化碳的质量=0.1mol×44g/mol=4.4g,
答:产生的CO2的质量为4.4g,需要HCl的物质的量为0.2mol.
点评:本题考查根据方程式的有关计算,比较基础,旨在考查学生对基础知识的理解掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
达平衡状态的可逆反应:N2(g)+3H2(g)?2NH3(g),改变某一条件,一段时间后,测得正反应速率以N2的浓度减小表示:v(N2)=0.6mol/(L?min),逆反应速率以NH3的浓度减小表示:v(NH3)=1.2mol/(L?min),此时可逆反应的状态是( )
| A、测定时,v正>v逆 |
| B、测定时,v正<v逆 |
| C、测定时,v正=v逆 |
| D、不可能达到新平衡 |
对于同一周期从左到右的主族元素,下列说法中正确的是( )
| A、原子半径逐渐减小 |
| B、元素的金属性逐渐增强 |
| C、最高正化合价逐渐增大 |
| D、单质的熔沸点逐渐降低 |
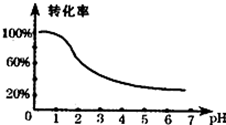
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )


| A、原子半径:Z>Y>X |
| B、R元素的含氧酸和W元素的含氧酸,酸性一定前者强 |
| C、X和Z形成的化合物能溶于NaOH溶液 |
| D、Y和W形成的化合物中,阴阳离子的个数可能比为1:1 |


 随着世界工业经济的发展、人口的剧增,全球能源紧张面临着越来越严重的问题,煤经过化学加工可转化为气体或液体以及各种化工产品,从而提高了煤的利用率.
随着世界工业经济的发展、人口的剧增,全球能源紧张面临着越来越严重的问题,煤经过化学加工可转化为气体或液体以及各种化工产品,从而提高了煤的利用率.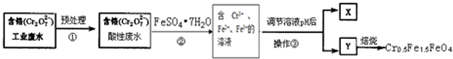
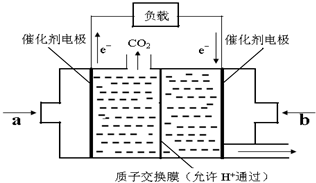
 已知B是一种由三种短周期(各位于不同周期)元素组成的正盐,该盐在常用锌锰干电池中做电解质:Y在常温下为液态,E的相同对分子质量比D大16,它们存在如下转化关系(反应条件及部分产物已略去);
已知B是一种由三种短周期(各位于不同周期)元素组成的正盐,该盐在常用锌锰干电池中做电解质:Y在常温下为液态,E的相同对分子质量比D大16,它们存在如下转化关系(反应条件及部分产物已略去);