题目内容
下述实验方案能达到实验目的是( )
| 选项 | A | B | C | D |
| 实验 方案 |  | 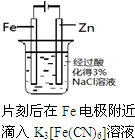 |  | 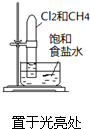 |
| 实验 目的 | 验证铁钉发生了 析氢腐蚀 | 验证Fe电极被保护 | 验证乙烯的产生 | 验证甲烷与氯气发生了化学反应 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.食盐水为中性,发生吸氧腐蚀;
B.Fe与电源正极相连;
C.乙烯、挥发的乙醇均能使酸性高锰酸钾氧化;
D.甲烷与氯气发生取代反应生成HCl,试管中液面上升.
B.Fe与电源正极相连;
C.乙烯、挥发的乙醇均能使酸性高锰酸钾氧化;
D.甲烷与氯气发生取代反应生成HCl,试管中液面上升.
解答:
解:A.食盐水为中性,发生吸氧腐蚀,而酸性溶液中发生析氢腐蚀,故A错误;
B.Fe与电源正极相连,作阳极,发生氧化反应,则Fe电极被腐蚀,故B错误;
C.乙烯、挥发的乙醇均能使酸性高锰酸钾氧化,不能验证乙烯的产生,应排除乙醇的干扰,故C错误;
D.甲烷与氯气发生取代反应生成HCl,试管中液面上升,实验装置可验证甲烷与氯气发生了化学反应,故D正确;
故选D.
B.Fe与电源正极相连,作阳极,发生氧化反应,则Fe电极被腐蚀,故B错误;
C.乙烯、挥发的乙醇均能使酸性高锰酸钾氧化,不能验证乙烯的产生,应排除乙醇的干扰,故C错误;
D.甲烷与氯气发生取代反应生成HCl,试管中液面上升,实验装置可验证甲烷与氯气发生了化学反应,故D正确;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,涉及电化学腐蚀、电解原理、常见有机物性质等,把握物质的性质及实验装置图的作用、反应原理为解答的关键,注意实验方案的评价性、操作性分析,题目难度不大.

练习册系列答案
相关题目
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
A、异戊二烯(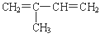 )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 |
| B、CH3CH2CH2Cl在碱性溶液中水解 |
| C、甲苯在一定条件下发生硝化生成一硝基甲苯的反应 |
| D、2-氯丁烷与NaOH乙醇溶液共热发生消去HCl分子的反应 |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )


| A、原子半径:Z>Y>X |
| B、R元素的含氧酸和W元素的含氧酸,酸性一定前者强 |
| C、X和Z形成的化合物能溶于NaOH溶液 |
| D、Y和W形成的化合物中,阴阳离子的个数可能比为1:1 |
下列各反应对应的离子方程式正确的是( )
| A、次氯酸钠溶液中通入过量二氧化硫ClO-+H2O+SO2→HClO+HSO3- |
| B、向碳酸氢钠溶液中加入过量氢氧化钙溶液2HCO3-+Ca2++2OH-→CaCO3↓+2H2O+CO32- |
| C、氢氧化钡溶液与硫酸溶液反应得到中性溶液Ba2++OH-+H++SO42-→BaSO4↓+H2O |
| D、50 mL 1mol/L的NaOH溶液中通入0.03mol H2S:5OH-+3H2S→HS-+2S2-+5H2O |
已知H2A为弱酸,下列说法错误的是( )
| A、0.1mol/L的Na2A溶液中:c(A2-)+c(HA-)+c(H2A)=0.1mol/L |
| B、常温下,将pH=3的H2A溶液稀释到原来的100倍,则稀释后溶液的pH<5 |
| C、常温下,将pH=3的H2A溶液与pH=11的NaOH溶液等体积混合,反应混合液呈酸性 |
| D、常温下,若1mol/L的NaHA溶液的pH=9,则溶液中:c(Na+)-c(HA-)-c(A2-)=10-5-10-9 |
下列气体中所含分子数目最多的是( )
| A、1g H2 |
| B、10g O2 |
| C、30gCl2 |
| D、17g NH3 |
常温下,2L物质的量浓度为0.5mol?L-1 KOH溶液含有( )
| A、1 mol的K+ |
| B、0.5 mol的H+ |
| C、1.0 mol的H+ |
| D、1.0 mol的OH- |
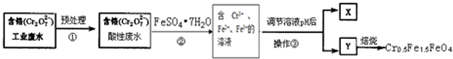
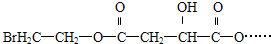
 )的原料,试写出其结构简式
)的原料,试写出其结构简式