题目内容
17.如图是化学反应中物质变化和能量变化的示意图.若E1>E2,则下列反应符合该示意图的是( )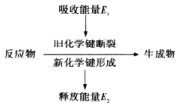
| A. | NaOH溶液与稀盐酸的反应 | B. | 锌与稀盐酸的反应 | ||
| C. | 氢氧化钡与氯化铵固体的反应 | D. | 一氧化碳在空气中的燃烧反应 |
分析 吸收能量E1大于E放出的能量E2,故为吸热反应,
根据常见的放热反应有:所有的物质燃烧、金属与酸或水反应、中和反应、铝热反应、绝大多数化合反应等,
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),八水合氢氧化钡与氯化铵的反应.
解答 解:吸收能量E1大于E放出的能量E2,故为吸热反应,
A.NaOH溶液与稀盐酸的反应属于放热反应,故A错误;
B.锌与稀盐酸的反应为放热反应,故B错误;
C.氢氧化钡与氯化铵固体的反应属于吸热反应,故C正确;
D.一氧化碳在空气中的燃烧反应属于放热反应,故D错误,
故选C.
点评 本题考查吸热反应和放热反应,难度不大,明确常见的吸热反应和放热反应是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.设NA为阿移伽德罗常数的值,下列说法正确的是( )
| A. | 1LpH=1的硫酸溶液中含有的H+数为0.2NA | |
| B. | 12g石墨和C60的混合物中质子总数为6NA | |
| C. | lmolNa2O2和足量的水完全反应,转移电子数为2NA | |
| D. | 2mol热的浓硫酸与足量Cu充分反应生成的SO2在标准状况下的体积约为22.4L |
8.一定条件想,将X和Y气体通入1L密闭容器中,发生反应:aX(g)+bY(g)?mZ(g),5s内反应速率如下:v(X)=0.3mol•L-1•s-1,v(Y)=0.6mol•L-1•s-1,v(Z)=0.6mol•L-1•s-1,则a、b、m的值分别为( )
| A. | 1、3、2 | B. | 1、2、2 | C. | 1、3、3 | D. | 1、1、3 |
5.下列对一些实验事实及其理论解释都正确的是( )
| 选项 | 实验事实 | 理论解释 |
| A | Be原子的第一电离能小于B原子 | 同周期元素原子的电离能随原子序数增大而增大 |
| B | CH4为正四面体形分子 | CH4分子中C为sp3杂化,键角为109°28′ |
| C | 金刚石的熔点高于石墨 | 金刚石是原子晶体,石墨是分子晶体 |
| D | HF的沸点高于HCl | HF分子间能形成氢键,HCl不能 |
| A. | A | B. | B | C. | C | D. | D |
12.在某元素的原子核外电子排布中,K电子层和L电子层的电子数之和等于M电子层和N电子层的电子数之和.则该元素的核电荷数为( )
| A. | 12 | B. | 17 | C. | 20 | D. | 30 |
9.在给定的条件下,下列选项所示的物质间转化均能实现的是( )
| A. | Al2O3$\stackrel{盐酸}{→}$AlCl3溶液$\stackrel{通电}{→}$Al | |
| B. | NH3$→_{△}^{O_{2}/催化剂}$NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| C. | S$→_{点燃}^{O_{2}}$SO2$\stackrel{H_{2}O}{→}$H2SO4 | |
| D. | SiO2$\stackrel{NaOH溶液}{→}$Na2SiO3溶液$\stackrel{CO_{2}}{→}$H2SiO3 |
 .
. $→_{②}^{NaOH,乙醇,△}$
$→_{②}^{NaOH,乙醇,△}$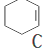 $→_{③}^{溴CCl_{4}溶液}$D$\stackrel{④}{→}$
$→_{③}^{溴CCl_{4}溶液}$D$\stackrel{④}{→}$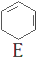
 ,名称是环己烷;
,名称是环己烷; ;B水解的化学方程式为
;B水解的化学方程式为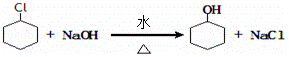 .
.