题目内容
2.(1)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术.太阳光分解海水时,光能转化为化学能,二氧化钛起催化剂作用.水分解时,断裂的化学键是极性共价键(填“离子键”、“极性共价键”、“非极性共价键”),分解海水的反应属于吸热反应(填“放热”或“吸热”).
(2)现有两个反应:①NaOH+HCl=NaCl+H2O,②Fe+H2SO4=FeSO4+H2↑.其中为放热反应的是①②,(填序号,下同)能设计成原电池的是②.
(3)ZnMnO2干电池应用广泛,其电解质溶液是ZnCl2NH4Cl混合溶液.
①该电池的负极材料是Zn,该电极反应式为Zn-2e-=Zn2+.
②若ZnCl2NH4Cl混合溶液中含有杂质Cu2+,会加速其电极的腐蚀,其主要原因是Zn+Cu2+=Zn2++Cu,形成原电池发生反应.
③欲除去Cu2+,最好选用下列试剂中的B(填代号).
A.NaOH B.Zn C.Fe D.NH3•H2O.
分析 (1)利用太阳能分解海水是将太阳能转化为化学能;氢氧燃料电池属于原电池,是将化学能转化为电能,断裂化学键需要吸收能量,形成化学键放出能量;
(2)大多数氧化还原反应和酸碱中和反应是放热反应;自发进行的放热的氧化还原反应能设计成原电池;
(3)①在氧化还原反应中失电子化合价升高的金属作负极、不如负极活泼的金属或导电的非金属作正极,得电子发生还原反应的电解质为该原电池电解质;
②锌比铜活泼,能置换出铜形成原电池加速锌的腐蚀;
③除杂时注意不能引入新的杂质.
解答 解:(1)科学家利用太阳能使海水分解,所以是太阳能转变为化学能,该反应中二氧化钛作催化剂;生成的氢气用于燃料电池时是把化学能转变为电能,水分解时,断裂的化学键是H-O共价键键;电解水是吸热反应,故答案为:化学;催化剂;极性共价键;吸热;
(2)大多数氧化还原反应和酸碱中和反应是放热反应,所以①②都是放热反应;自发进行的放热的氧化还原反应能设计成原电池,②是自发的氧化还原反应,故答案为:①②;②;
(3)①Zn-MnO2干电池中,活泼金属锌做原电池的负极,电极反应式为:Zn-2e-=Zn2+,故答案为:Zn,Zn-2e-=Zn2+;
②锌比铜活泼,能置换出铜,反应为Zn+Cu2+=Zn2++Cu,形成原电池加速锌的腐蚀,故答案为:Zn+Cu2+=Zn2++Cu,形成原电池发生反应;
③A、C、D都引入新的杂质离子,除杂时注意不能引入新的杂质只有B符合,故答案为:B.
点评 本题考查原电池的工作原理,题目难度不大,注意基础知识的积累.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
13.化学与我们人类生活息息相关,下列说法不正确的是( )
| A. | 开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 | |
| B. | 工业上,电解熔融MgCl2制金属镁 | |
| C. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| D. | “冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高 |
10.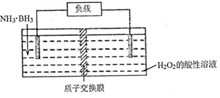 氨硼烷(NH3•BH3)电池可在常温下工作,装置如图所示.该电池工作时的总反应为:NH3•BH3+3H2O2=NH4BO2+4H2O.下列说法正确的是( )
氨硼烷(NH3•BH3)电池可在常温下工作,装置如图所示.该电池工作时的总反应为:NH3•BH3+3H2O2=NH4BO2+4H2O.下列说法正确的是( )
 氨硼烷(NH3•BH3)电池可在常温下工作,装置如图所示.该电池工作时的总反应为:NH3•BH3+3H2O2=NH4BO2+4H2O.下列说法正确的是( )
氨硼烷(NH3•BH3)电池可在常温下工作,装置如图所示.该电池工作时的总反应为:NH3•BH3+3H2O2=NH4BO2+4H2O.下列说法正确的是( )| A. | 负极附近溶液的PH增大 | |
| B. | 正极的反应式为:H2O2+2H++2e-=2H2O | |
| C. | 电池工作时,BO2-通过质子交换膜向正极移动 | |
| D. | 消耗3.lg氨硼烷,理论上转移0.2mol电子 |
17.如图是化学反应中物质变化和能量变化的示意图.若E1>E2,则下列反应符合该示意图的是( )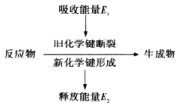

| A. | NaOH溶液与稀盐酸的反应 | B. | 锌与稀盐酸的反应 | ||
| C. | 氢氧化钡与氯化铵固体的反应 | D. | 一氧化碳在空气中的燃烧反应 |
7.莽草酸结构简式如图,有关说法正确的是( )
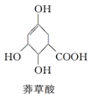

| A. | 分子中含有2种官能团 | |
| B. | 1mol莽草酸与Na反应最多生成4mol氢气 | |
| C. | 可与乙醇、乙酸反应,且反应类型相同 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |
14.下列化学用语或物质结构的表述正确的是( )
| A. | 中子数为10 的氧原子:10O | |
| B. | 过氧化氢的电子式:H-O-O-H | |
| C. | CS2中各原子最外层都满足8 电子结构 | |
| D. | CH2Cl2是四面体构型的含非极性健的分子 |
6.常温下,将足量的AgCl固体分别放入下列液体中,AgCl的溶解度由大到小排列的顺序正确的是( )
①20mL蒸馏水
②30mL 0.03mol/L HCl溶液
③40mL 0.05mol/L AgNO3溶液
④50mL 0.02mol/L CaCl2溶液.
①20mL蒸馏水
②30mL 0.03mol/L HCl溶液
③40mL 0.05mol/L AgNO3溶液
④50mL 0.02mol/L CaCl2溶液.
| A. | ②>④>③>① | B. | ①>②>④>③ | C. | ①>②>③>④ | D. | ③>②>④>① |
7.水杨酸、冬青油、阿司匹林都是常用西药,它们的结构简式如表:以下说法不正确的是( )
| 有机物 | 水杨酸 | 冬青油 | 阿司匹林 |
结构简式 |  |  | 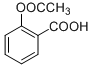 |
| A. | 可以用FeCl3溶液鉴别冬青油和阿司匹林 | |
| B. | 由水杨酸制冬青油的反应是取代反应 | |
| C. | 1mol阿司匹林最多能与3 mol NaOH反应 | |
| D. | 可以用碳酸钠溶液除去冬青油中少量的水杨酸 |