题目内容
19.现有下列十种物质:①H2②铝③CaO④CO2⑤H2SO4 ⑥Ba(OH)2⑦红褐色的氢氧化铁液体⑧氨水⑨稀硝酸⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 |
(3)⑩在水中的电离方程式为Al2(SO4)3=2Al3++2SO42-,
(4)少量的④通入⑥的溶液中反应的离子方程式为CO2+Ba2++2OH-=BaCO3↓+H2O.
(5)②与⑨发生反应的化学方程式为:Al+4HNO3═Al(NO3)3+NO↑+2H2O,该反应的氧化剂是HNO3(填化学式),氧化剂与还原剂的物质的量之比是1:1,当有5.4gAl发生反应时,转移电子的物质的量为0.6mol.该反应的离子方程式为Al+4H++NO3-=Al3++NO↑+2H2O.
(6)白色沉淀变成灰绿色再变成红褐色沉淀的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
分析 (1)根据物质的分类标准和物质所属的类别来回答;
(2)发生离子反应:H++OH-=H2O,是强酸强碱发生反应生成溶于水的盐;
(3)Al2(SO4)3属于盐是强电解质,水溶液中完全电离;
(4)少量的④通入⑥的溶液中反应,是二氧化碳通入氢氧化钡溶液中反应生成碳酸钡沉淀和水;
(5)依据化学方程式中元素化合价变化分析,元素化合价降低的物质做氧化剂,元素化合价升高的物质做还原剂,依据电子守恒计算氧化剂和还原剂物质的量之比,电子转移总数,硝酸和硝酸铝都是强电解质完全电离,几次写出反应的离子方程式;
(6)氢氧化亚铁在空气中被氧化成氢氧化铁,所以会出现白色沉淀迅速变成灰绿色、最终变成红褐色的现象,据此写出反应的化学方程式.
解答 解:(1)铝是只有金属铝元素组成的金属单质,③Na2O和④CO2中含有两种元素其中一种元素是氧元素,属于氧化物,⑧氨水和⑨稀硝酸属于混合物,⑦红褐色的氢氧化铁液体属于胶体分散系,③⑤⑥⑩在水溶液或者熔融状态下能导电,属于电解质,
故答案为:
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 | ② | ③④ | ⑧⑨ | ⑦ | ③⑤⑥⑩ |
故答案为:Ba(OH)2+2HNO3=Ba(NO3)2+2H2O;
(3)Al2(SO4)3属于盐是强电解质,水溶液中完全电离,电离方程式为:Al2(SO4)3=2Al3++2SO42-;
故答案为:Al2(SO4)3=2Al3++2SO42-;
(4)少量的④通入⑥的溶液中反应,是二氧化碳通入氢氧化钡溶液中反应生成碳酸钡沉淀和水,反应的离子方程式为:CO2+Ba2++2OH-=BaCO3↓+H2O;
故答案为;CO2+Ba2++2OH-=BaCO3↓+H2O;
(5)②与⑨发生反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,反应中氮元素化合价从+5价变化为+2价,化合价降低硝酸做氧化剂,该反应的氧化剂是HNO3;依据电子守恒可知1molAl全部反应,氧化剂和还原剂转移电子总数为3mol,氧化剂和还原剂物质的量之比为1:1;当有5.4g Al物质的量=$\frac{5.4g}{27g/mol}$=0.2mol,发生反应电子转移0.6mol,反应的离子方程式为:Al+4H++NO3-=Al3++NO↑+2H2O;
故答案为:HNO3;1:1;0.6mol;Al+4H++NO3-=Al3++NO↑+2H2O;
(6)氢氧化亚铁不稳定,在空气中很容易被氧化成氢氧化铁,所以白色沉淀迅速变成灰绿色最后变成红褐色,反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评 本题考查了物质分类的依据,化学方程式、离子方程式书写方法,物质组成和性质是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7. 美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
 美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )| A. | a极为电池的正极 | |
| B. | b极发生氧化反应 | |
| C. | 负极的反应为:4H++O2+4e-═2H2O | |
| D. | 电池工作时,1mol乙醇被氧化时有12mol转移 |
4.下图所示的实验操作,不能达到相应目的是( )
| A. | 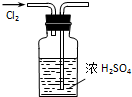 干燥Cl2 | B. | 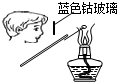 检验K2CO3中的K+ | ||
| C. | 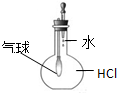 证明HCl极易溶于水 | D. |  实验室制氨气 |
9.二氧化硫、二氧化碳、三氧化硫同时具备的性质是( )
| A. | 都能使品红试液褪色 | |
| B. | 都能和氢氧化钠溶液反应生成盐和水 | |
| C. | 都有刺激性气味 | |
| D. | 常温下都是气体 |
 金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速.完成下列填空:
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速.完成下列填空: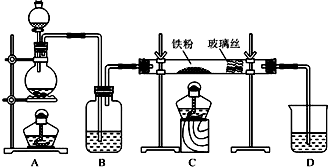

 (R、R′代表烃基)
(R、R′代表烃基)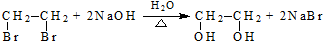 .
. .
. (C10H10O4)的同分异构体中,满足下列条件的有5种.
(C10H10O4)的同分异构体中,满足下列条件的有5种.