题目内容
11.将甲盐溶液与稀硫酸混合,产生气体X和黄色单质Y.将气体X通入足量乙溶液中,取反应后溶液滴加BaCl2溶液产生白色沉淀.则:(1)单质Y的元素位于周期表中第三周期,ⅥA族;
(2)甲盐与稀硫酸反应的离子方程式为S2O32-+2H+=S↓+SO2↑+H2O;
(3)乙溶液可能是下列物质中的ABC(填选项字母).
A.H2O2 B.Na2SO4 C.氨水 D.FeCl2.
分析 将甲盐溶液与稀硫酸混合,产生气体X和黄色单质Y,则甲为Na2S2O3,X为SO2、Y为S,将气体X(SO2)通入足量乙溶液中,取反应后溶液滴加BaCl2溶液产生白色沉淀,说明生成BaSO4或BaSO3,乙溶液可能具有强氧化性或碱性,可能为选项中的H2O2、氨水、FeCl3,而硫酸钠能与氯化钡反应生成硫酸钡,故也可能为硫酸钠溶液.
解答 解:将甲盐溶液与稀硫酸混合,产生气体X和黄色单质Y,则甲为Na2S2O3,X为SO2、Y为S.
(1)Y为S,硫元素处于第三周期ⅥA族,故答案为:三;ⅥA;
(2)甲盐与稀硫酸反应的离子方程式为:S2O32-+2H+=S↓+SO2↑+H2O,故答案为:S2O32-+2H+=S↓+SO2↑+H2O;
(3)将气体X(SO2)通入足量乙溶液中,取反应后溶液滴加BaCl2溶液产生白色沉淀,说明生成BaSO4或BaSO3,乙溶液可能具有强氧化性或碱性,可能为选项中的H2O2、氨水,而硫酸钠能与氯化钡反应生成硫酸钡,故也可能为硫酸钠溶液,FeCl2不能氧化二氧化硫,故答案为:ABC.
点评 本题考查无机物推断,为高频考点,侧重于学生的分析能力的考查,中学对硫代硫酸钠涉及较少,难度较大,(3)为易错点,学生容易忽略硫酸钠溶液.

练习册系列答案
相关题目
17.某有机物的分子式为C9H12,其属于芳香烃的同分异构体有(不考虑、立体异构)( )
| A. | 5 种 | B. | 6 种 | C. | 7 种 | D. | 8 种 |
19.现有下列十种物质:
①H2②铝③CaO④CO2⑤H2SO4 ⑥Ba(OH)2⑦红褐色的氢氧化铁液体⑧氨水⑨稀硝酸⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-═H2O,该离子反应对应的化学方程式为Ba(OH)2+2HNO3=Ba(NO3)2+2H2O.
(3)⑩在水中的电离方程式为Al2(SO4)3=2Al3++2SO42-,
(4)少量的④通入⑥的溶液中反应的离子方程式为CO2+Ba2++2OH-=BaCO3↓+H2O.
(5)②与⑨发生反应的化学方程式为:Al+4HNO3═Al(NO3)3+NO↑+2H2O,该反应的氧化剂是HNO3(填化学式),氧化剂与还原剂的物质的量之比是1:1,当有5.4gAl发生反应时,转移电子的物质的量为0.6mol.该反应的离子方程式为Al+4H++NO3-=Al3++NO↑+2H2O.
(6)白色沉淀变成灰绿色再变成红褐色沉淀的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
①H2②铝③CaO④CO2⑤H2SO4 ⑥Ba(OH)2⑦红褐色的氢氧化铁液体⑧氨水⑨稀硝酸⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 |
(3)⑩在水中的电离方程式为Al2(SO4)3=2Al3++2SO42-,
(4)少量的④通入⑥的溶液中反应的离子方程式为CO2+Ba2++2OH-=BaCO3↓+H2O.
(5)②与⑨发生反应的化学方程式为:Al+4HNO3═Al(NO3)3+NO↑+2H2O,该反应的氧化剂是HNO3(填化学式),氧化剂与还原剂的物质的量之比是1:1,当有5.4gAl发生反应时,转移电子的物质的量为0.6mol.该反应的离子方程式为Al+4H++NO3-=Al3++NO↑+2H2O.
(6)白色沉淀变成灰绿色再变成红褐色沉淀的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
6.无机化合物可根据其组成和性质进行分类,如:
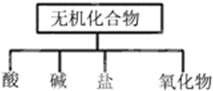
(1)如图所示的物质分类方法名称是树状分类法.
(2)以Na、K、H、O、C、S、N中任意两种或三种元素组成合适的物质,分别填在下表②③⑥的后面.
(3)写出⑦转化为⑤的化学方程式Na2O+CO2═Na2CO3.
(4)实验室制备⑦检验该气体的方法是将气体通入澄清的石灰水中,变浑浊,则说明该气体是二氧化碳.

(1)如图所示的物质分类方法名称是树状分类法.
(2)以Na、K、H、O、C、S、N中任意两种或三种元素组成合适的物质,分别填在下表②③⑥的后面.
| 物质 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ②HNO3 | ③NaOH、KOH或NH3•H2O ④Ba(OH)2 | ⑤Na2CO3 ⑥NaNO3、Na2SO4或NH4NO3 | ⑦CO2 ⑧Na2O |
(4)实验室制备⑦检验该气体的方法是将气体通入澄清的石灰水中,变浑浊,则说明该气体是二氧化碳.
16.下列有关物质用途的说法正确的是( )
| A. | 氯气可用于自来水消毒 | B. | 甲醛可用作食品防腐剂 | ||
| C. | 碳酸钠可用来治疗胃酸过多 | D. | 铝制容器可长期存放碱性物质 |
3.1mol某气态烃能与1mol氯化氢发生加成反应,加成后的产物又可与7mol氯气发生完全的取代反应,则该烃的结构简式为( )
| A. | CH2═CH2 | B. | CH3CH═CH2 | C. | CH3CH2CH═CH2 | D. | CH3CH2CH2CH═CH2 |
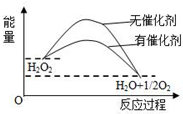
20.已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示.下列说法正确的是( )

| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热化学方程式:H2O2=H2O+$\frac{1}{2}$O2+Q | |
| D. | 反应物的总能量高于生成物的总能量 |
1.下列各组中的两种物质发生变化时,所克服的作用力属于同种类型的是( )
| A. | 二氧化硅和氯化镁熔化 | B. | 碘和氯化铵受热变成气体 | ||
| C. | 水和干冰的气化 | D. | 氯化钠和氯化氢溶于水 |
