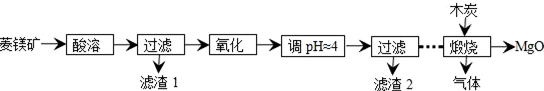
题目内容
19. 在周期表中1~36号之间的A、B、C、D、E、F六种元素,它们的原子序数依次增大,已知A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E的基态原子中未成对电子数是核外电子总数的$\frac{1}{4}$,F元素位于周期表的ds区,其基态原子最外能层只有一个电子.
在周期表中1~36号之间的A、B、C、D、E、F六种元素,它们的原子序数依次增大,已知A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E的基态原子中未成对电子数是核外电子总数的$\frac{1}{4}$,F元素位于周期表的ds区,其基态原子最外能层只有一个电子.(1)写出基态E原子的价电子排布图3d54s1.
(2)B、C、D三种元素第一电离能由小到大的顺序为C<O<N(用元素符号表示).
(3)B的最高价氧化物对应的水化物分子中,中心原子的杂化类型为sp2杂化,C的单质与化合物BD是等电子体,根据等电子体原理,写出化合物BD的电子式
 .
.(4)A2D的沸点在同族元素中最高,其原因是由于水分子间形成氢键,导致沸点升高.A2D由液态形成晶体时密度减小(填“增大”、“不变”或“减小”),其主要原因水形成晶体时,每个水分子与4个水分子形成氢键,构成空间正四面体网状结构,水分子空间利用率低,密度反而减小.(用文字叙述).
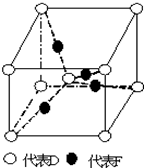
(5)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为Cu2O.(用元素符号表示)
若相邻D原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为$\frac{27\sqrt{3}}{2{N}_{A}{a}^{3}}$g.cm-3(用含a、NA的符号表示).
分析 在元素周期表前四周期中原子序数依次增大的六种元素A、B、C、D、E、F中,B的一种核素在考古时常用来鉴定一些文物的年代,则B为C元素,D原子核外电子有8种不同的运动状态,则D为O元素,C元素原子的最外层有3个自旋方向相同的未成对电子,且C的原子序数小于D,所以C为N元素,E元素在第四周期,E的基态原子中未成对电子数是核外电子总数的1/4,其原子外围电子排布式为1s22s22p63s23p63d54s1,则E为Cr元素,F元素位于周期表的ds区,其基态原子最外能层只有一个电子,则F原子外围电子排布为3d104s1,所以F为Cu元素,A与其余五种元素既不同周期也不同主族,所以A为H元素,以此解答该题.
解答 解:(1)E为铬元素,基态E原子的价电子排布式3d54s1,
故答案为:3d54s1;
(2)C、O、N元素都是第二周期非金属元素,同一周期元素自左而右第一电离能呈增大趋势,但N元素原子2p能级是半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能C<O<N,故答案为:C<O<N;
(3)B为C元素,最高价氧化物对应的水化物为碳酸,分子中,中心原子C形成3个δ键,没有孤电子对,为sp2杂化,氮的单质与CO是等电子体,据等电子体的原理,CO的电子式为 ,
,
故答案为:sp2杂化; ;
;
(4)H2O由于水分子间形成氢键,导致沸点升高,由液态形成晶体时密度会减小,因为水分子之间形成氢键,氢键有方向性,每个水分子与4个水分子形成氢键,构成空间正四面体网状结构,水分子空间利用率低,使分子之间的间隙变大,密度反而减小,
故答案为:由于水分子间形成氢键,导致沸点升高; 减小;水形成晶体时,每个水分子与4个水分子形成氢键,构成空间正四面体网状结构,水分子空间利用率低,密度反而减小;
(5)根据晶胞的结构图可知,晶胞中含有氧原子数为$8×\frac{1}{8}+1$=2,铜原子数为4,所以该化合物的化学式为Cu2O,若相邻氧原子和铜原子间的距离为a cm,则晶胞的体对角线为4acm,所以边长为$\frac{4}{\sqrt{3}}a$cm,所以体积为$(\frac{4}{\sqrt{3}}a)^{3}$cm3,该晶体的密度为 $\frac{\frac{64×4+16×2}{{N}_{A}}}{(\frac{4}{\sqrt{3}}a)^{3}}$g/cm3=$\frac{27\sqrt{3}}{2{N}_{A}{a}^{3}}$g/cm3(用含a、NA的符号表示),
故答案为:Cu2O;$\frac{27\sqrt{3}}{2{N}_{A}{a}^{3}}$.
点评 本题主要考查较为综合,涉及物质结构与性质以及晶胞的计算,为高考常见题型,题目侧重于考查原子核外电子排布、第一电离能、原子杂化、等电子体、氢键、晶胞的计算等知识点,中等难度,元素推断是解题的关键,答题时注意物质结构知识的灵活运用.

| A. | 25℃、101KPa时,16g O2和O3混合气体中含有的原子数为NA | |
| B. | 1 mol NH3中含有的质子数为17NA | |
| C. | 11.2 L O2和N2的混合气体含有的分子数为0.5NA | |
| D. | 金属铁与稀盐酸反应当产生0.1 mol H2时转移电子数为0.3NA |
| A. | MnO2→Mn2+ | B. | CO→CO2 | C. | Cu→Cu2+ | D. | Cl2→Cl- |

| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戍醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热A,回流50min.反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是球形冷凝管.
(2)在洗涤操作中,第一次水洗的主要目的是洗掉大部分硫酸和醋酸,第二次水洗的主要目的是洗掉碳酸氢钠.
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是提高醇的转化率.
(5)实验中加入少量无水MgSO4的目的是干燥.
(6)在蒸馏操作中,仪器选择及安装都正确的是b(填标号).
(7)本实验的产率是c(填标号).
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”),其原因是会收集少量未反应的异戊醇.
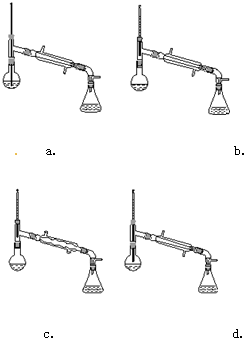
| A. | ①③⑤ | B. | ①②③ | C. | ②④ | D. | ①③④⑤ |
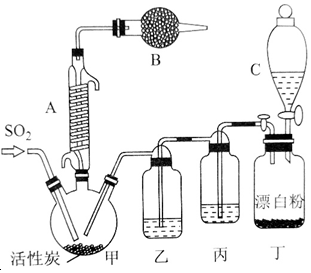 有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解.回答下列问题:
有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解.回答下列问题: