题目内容
9.标准状况下,①4g氢气、②33.6L甲烷(CH4)、③6.02×1023个水分子中,含原子数最多的是②(填序号).分析 根据N=nNA可知,原子的物质的量越多,则含有原子数越多;分别计算出各物质中含有原子的物质的量,根据计算结果进行判断.
解答 解:①4g氢气的物质的量为:$\frac{4g}{2g/mol}$=2mol,2mol氢气分子中含有H原子的物质的量为:2mol×2=4mol;
②标准状况下33.6L甲烷(CH4)的物质的量为:$\frac{33.6L}{22.4L/mol}$=1.5mol,1.5mol甲烷分子中含有原子的物质的量为:1.5mol×5=7.5mol;
③6.02×1023个水分子的物质的量为:$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=1mol,1mol水分子中含有原子的物质的量为:1mol×3=3mol;
根据N=nNA可知,原子的物质的量越多,则含有原子数越多,则含有原子数最多的为②,
故答案为:②.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数、气体摩尔体积之间的关系为解答关键,试题侧重基础知识的考查,有利于提高学生的化学计算能力.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案
相关题目
19.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 将稀硫酸和Na2S反应生成的气体通入AgNO3与AgCl组成的浊液中 | Ksp(AgCl)>Ksp(Ag2S) |
| B | 室温下,向浓度均为0.1 mol•L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀. | Ksp(BaSO4)<Ksp(CaSO4) |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色. | Fe3+的氧化性比I2的强 |
| D | 室温下,用pH试纸测得0.1mol•L-1 Na2SO3溶液的pH约为10;0.1mol•L-1 NaHSO3溶液的pH约为5. | HSO3-结合H+的能力比SO32-的强 |
| A. | A | B. | B | C. | C | D. | D |
17.在pH=1溶液中能大量共存的是( )
| A. | Na+、SO42-、Ba2+、Cl- | B. | Na+、K+、CH3COO-、NO3- | ||
| C. | H+、Cu2+、OH-、CO32- | D. | K+、Na+、Cl-、NO3- |
4.下列事实能说明相应的酸是弱电解质的是( )
| A. | 用HR做导电实验,灯泡很暗 | |
| B. | 0.1mol•L-1HR溶液稀释到100倍时,溶液的pH值为3 | |
| C. | 20mL0.1mol•L-1HR恰好中和20mL0.1mol•L-1NaOH溶液 | |
| D. | 0.1mol•L-1NH4R溶液的pH等于7 |
14.下列实验装置及操作 (略去部分夹持仪器)正确的是( )
| A. |  观察Fe(OH)2的生成 | B. |  中和滴定 | ||
| C. |  除去CO2气体中的HCl气体 | D. | 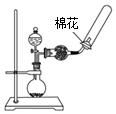 制取并收集干燥的氨气 |
1.下列物质中,属于纯净物的是( )
| A. | 白酒 | B. | 石灰石 | C. | 冰水 | D. | 矿泉水 |
18.关于同温、同压下等体积的CO2和CO的叙述,其中正确的是( )
①质量相等;②密度相等;③所含分子个数相等;④所含碳原子个数相等.
①质量相等;②密度相等;③所含分子个数相等;④所含碳原子个数相等.
| A. | ①②③④ | B. | ②③④ | C. | 只有③④ | D. | 只有④ |
4.下列递变规律不正确的是( )
| A. | Na、Mg、Al原子的失电子能力逐渐减弱 | |
| B. | Si、P、S元素的最高正化合价依次降低 | |
| C. | C、N、O的原子半径依次减小 | |
| D. | Cl、Br、I的气态氢化物的稳态性依次减弱 |