题目内容
7.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 4℃时,18g 21H2168O中含有电子数为10NA | |
| B. | 在密闭容器中加入1.5 mol H2和0.5 molN2,充分反应后可得到NH3分子数为NA | |
| C. | 常温下,1L0.1mol•L-1的NH4NO3溶液中所含氮原子数为0.2 NA | |
| D. | 标准状况下,22.4 L的CCl4中C-Cl键数为4NA |
分析 A、21H2168O的摩尔质量为20g/mol;
B、合成氨的反应为可逆反应;
C、1mol硝酸铵中含2molN原子;
D、标况下四氯化碳为液态.
解答 解:A、21H2168O的摩尔质量为20g/mol,故18g21H2168O的物质的量为0.9mol,故含9NA个电子,故A错误;
B、合成氨的反应为可逆反应,不能进行彻底,故生成的氨气分子小于NA个,故B错误;
C、1mol硝酸铵中含2molN原子,虽然铵根离子在溶液中能水解,但根据原子守恒可知,故在1L0.1mol•L-1的NH4NO3溶液中所含氮原子数为0.2NA,故C正确;
D、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量和C-Cl键个数,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
18.a、b、c、d为原子序数依次增大的短周期主族元素,其最外层电子数之和为20,a是第二周期元素,c原子最外层电子数既是a原子内层电子总数的3倍,又是b原子最外层电子数的2倍,下列说法正确的是( )
| A. | 原子半径:d>b | |
| B. | 最高价氧化物对应水化物的酸性:d>c | |
| C. | 化合物ac2中含有离子键 | |
| D. | 氧元素分别与a、b形成的化合物都是共价化合物 |
15.1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素教案的内在联系,成为化学史上的重要里程碑之一.下列有关元素周期表的说法正确的是( )
| A. | 第ⅠA族的元素全部是金属元素 | |
| B. | 元素周期表有18个纵行,即18个族 | |
| C. | 短周期是第一、二、三、四周期 | |
| D. | 元素周期表有七个横行,也是七个周期 |
2.有机化学中取代反应范畴很广,下列反应中,属于取代反应范畴的是( )
| A. | CH2═CH2+Br2→CH2Br-CH2Br | B. | CH3CH2CHO+HCN→CH3CH2CH(CN)OH | ||
| C. | CH3CH2OH→CH2=CH2↑+H2O | D. | CH3CH2OH+HBr→CH3CH2Br+H2O |
12.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,下列叙述不正确的是( )
| A. | 原子半径B>A>C>D | B. | 原子序数 a>b>c>d | ||
| C. | 离子半径C3->D->B+>A2+ | D. | 离子的还原性C3->D- |
16.下列物质的鉴别和分离方法正确的是( )
| A. | 用氨水鉴别Al3+、Mg2+和Ag+ | |
| B. | 用加热法分离NH4Cl和I2 | |
| C. | 用无水乙醇提取碘水中的单质碘 | |
| D. | 用饱和Na2CO3溶液鉴别乙酸和乙酸乙酯 |
17.既发生了化学反应,又有电解质的溶解过程,且这两个过程都吸热的是( )
| A. | 冰醋酸与NaOH溶液反应 | B. | KNO3加入水中 | ||
| C. | NH4NO3加入水中 | D. | CaO加入水中 |
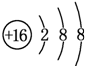 ;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e-稳定结构,电子式为
;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e-稳定结构,电子式为 .
.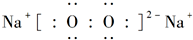 .
.