题目内容
17.反应3A(g)+B(g)→2C(g),若2min内A由1.2mol/L变为0.6mol/L则:v(A)=0.3mol/(L.min),v(B)=0.1mol/(L.min),v(C)=0.2mol/(L.min).分析 先根据v=$\frac{△c}{△t}$计算A的平均反应速率,同一可逆反应中同一段时间内,各物质的反应速率之比等于其计量数之比,据此计算B、C反应速率.
解答 解:v(A)=$\frac{△c}{△t}$=$\frac{1.2-0.6}{2}$mol/(L.min)=0.3mol/(L.min),同一可逆反应中同一段时间内,各物质的反应速率之比等于其计量数之比,所以v(B)=$\frac{1}{3}$v(A)=$\frac{1}{3}$×0.3mol/(L.min)=0.1mol/(L.min),v(C)=$\frac{2}{3}$v(A)=$\frac{2}{3}$×0.3mol/(L.min)=0.2mol/(L.min),
故答案为:0.3mol/(L.min);0.1mol/(L.min);0.2mol/(L.min).
点评 本题考查化学反应速率的有关计算,为高频考点,侧重考查学生计算能力,明确化学计量数与反应速率关系是解本题关键,题目难度不大.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
7.将足量的铜屑加入到浓度均为2mol/L的HNO3和H2SO4的混合溶液100mL中,充分反应后,转移电子的物质的量为( )
| A. | 0.6 mol | B. | 0.4 mol | C. | 0.8 mol | D. | 0.45mol |
12.NA为阿伏伽德罗常数的值.下列说法不正确的是( )
| A. | 10gH218O与10gD2O所含的中子数均为5NA | |
| B. | 1L0.1mol•L-1NH4Cl溶液所含NH4+数为0.1NA | |
| C. | 2.4gMg在空气中充分燃烧,转移电子数为0.2NA | |
| D. | 100g质量分数为46%的酒精水溶液中含氧原子总数为4NA |
6.欲从苯酚的乙醇洛液中分离苯酚和乙醇,有下列操作:①蒸馏 ②过滤③静置分液④加入足量的金属钠⑤通入过量的二氧化碳⑥加入足且的NaOH溶液⑦加入足量的FeC13溶液⑧加入乙酸和浓硫酸的混合液加热.合理合理的实验操作步骤及顺序是( )
| A. | ④⑤③ | B. | ⑥①⑤③ | C. | ⑧①⑦③ | D. | ⑤②⑥③ |
7.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 4℃时,18g 21H2168O中含有电子数为10NA | |
| B. | 在密闭容器中加入1.5 mol H2和0.5 molN2,充分反应后可得到NH3分子数为NA | |
| C. | 常温下,1L0.1mol•L-1的NH4NO3溶液中所含氮原子数为0.2 NA | |
| D. | 标准状况下,22.4 L的CCl4中C-Cl键数为4NA |
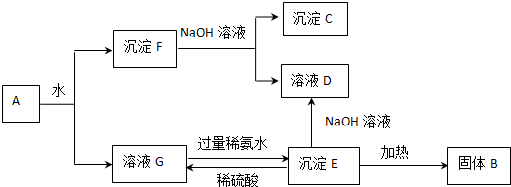
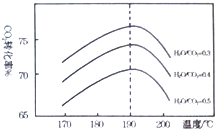 二氧化碳是一种宝贵的碳氧资源.以C02和NH3
二氧化碳是一种宝贵的碳氧资源.以C02和NH3