题目内容
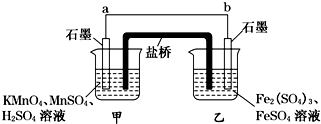
课题式研究性学习是培养学生创造性思维的良好方法,某研究性学习小组将下列装置如图链接,C、D、E、F、X、Y都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附件先显红色.试回答下列问题:
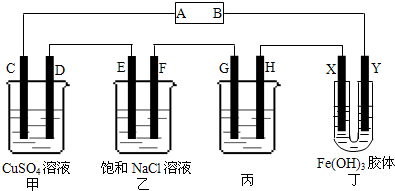
(1)电源A极的名称是 .
(2)甲装置中电解反应的总化学方程式: .
(3)如果收集乙装置中产生的气体,相同状况下两种气体的体积比是 .
(4)欲用丙装置给铜镀银,G应该是 (填“铜”或“银”),电镀液的溶质是 (填化学式).
(5)装置丁中的现象是 .

(1)电源A极的名称是
(2)甲装置中电解反应的总化学方程式:
(3)如果收集乙装置中产生的气体,相同状况下两种气体的体积比是
(4)欲用丙装置给铜镀银,G应该是
(5)装置丁中的现象是
考点:原电池和电解池的工作原理
专题:电化学专题
分析:将电源接通后,向乙中滴入酚酞试液,在F极附件先显红色,说明F电极为阴极,则E为阳极,所以C、G、X都是阳极,D、H、Y都是阴极,
(1)连接阴极的电极负极、连接阳极的电极是正极;
(2)甲中阳极上氢氧根离子放电、阴极上铜离子放电;
(3)乙中阳极上氯离子放电生成氯气、阴极上氢离子放电生成氢气,生成相同物质的量的氢气、氯气时转移电子相等,电解过程中转移电子总数相等,所以生成氢气、氯气物质的量相等;
(4)电镀时,镀层作阳极、镀件作阴极,电解质为可溶性的盐且含有的金属元素与阳极材料相同;
(5)氢氧化铁胶粒带正电荷,通电时向阴极移动.
(1)连接阴极的电极负极、连接阳极的电极是正极;
(2)甲中阳极上氢氧根离子放电、阴极上铜离子放电;
(3)乙中阳极上氯离子放电生成氯气、阴极上氢离子放电生成氢气,生成相同物质的量的氢气、氯气时转移电子相等,电解过程中转移电子总数相等,所以生成氢气、氯气物质的量相等;
(4)电镀时,镀层作阳极、镀件作阴极,电解质为可溶性的盐且含有的金属元素与阳极材料相同;
(5)氢氧化铁胶粒带正电荷,通电时向阴极移动.
解答:
解:将电源接通后,向乙中滴入酚酞试液,在F极附件先显红色,说明F电极为阴极,则E为阳极,所以C、G、X都是阳极,D、H、Y都是阴极,
(1)连接阴极的电极负极、连接阳极的电极是正极,A连接阳极,则为正极,故答案为:正极;
(2)甲中阳极上氢氧根离子放电、阴极上铜离子放电生成铜,所以电池反应式为2CuSO4+2H2O
2Cu+O2↑+H2SO4,故答案为:2CuSO4+2H2O
2Cu+O2↑+H2SO4;
(3)乙中阳极上氯离子放电生成氯气、阴极上氢离子放电生成氢气,生成相同物质的量的氢气、氯气时转移电子相等,电解过程中转移电子总数相等,所以生成氢气、氯气物质的量相等,相同条件下气体的物质的量之比等于体积之比,所以氯气和氢气体积之比为1:1,故答案为:1:1;
(4)欲用丙装置给铜镀银,Ag作阳极、Cu作阴极,则G为银,电解质为AgNO3,故答案为:银;AgNO3;
(5)氢氧化铁胶粒带正电荷,通电时向阴极移动,Y为阴极,所以看到的现象是Y极附近红褐色变深,故答案为:Y极附近红褐色变深.
(1)连接阴极的电极负极、连接阳极的电极是正极,A连接阳极,则为正极,故答案为:正极;
(2)甲中阳极上氢氧根离子放电、阴极上铜离子放电生成铜,所以电池反应式为2CuSO4+2H2O
| ||
| ||
(3)乙中阳极上氯离子放电生成氯气、阴极上氢离子放电生成氢气,生成相同物质的量的氢气、氯气时转移电子相等,电解过程中转移电子总数相等,所以生成氢气、氯气物质的量相等,相同条件下气体的物质的量之比等于体积之比,所以氯气和氢气体积之比为1:1,故答案为:1:1;
(4)欲用丙装置给铜镀银,Ag作阳极、Cu作阴极,则G为银,电解质为AgNO3,故答案为:银;AgNO3;
(5)氢氧化铁胶粒带正电荷,通电时向阴极移动,Y为阴极,所以看到的现象是Y极附近红褐色变深,故答案为:Y极附近红褐色变深.
点评:本题考查电解原理,正确判断阴阳极是解本题关键,知道各个电极上发生的反应,会正确书写电极反应式,难点是进行有关计算,(5)的现象能说明氢氧化铁胶粒带正电荷.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉淀,则通入的气体可能是( )
| A、CO2 |
| B、NH3 |
| C、SO3 |
| D、Cl2 |
下列涉及有机物的性质的说法错误的是( )
| A、乙烯和聚氯乙烯都能发生加成反应 |
| B、将铜丝在酒精灯上加热后,立即伸人无水乙醇中,铜丝恢复成原来的红色 |
| C、黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了 |
| D、乙烯和苯都使溴水褪色,但褪色的原理不相同 |
在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积缩小一半,当达到新平衡时,B的浓度是原来的1.8倍,则( )
| A、平衡向正反应方向移动了 |
| B、物质A的转化率增大了 |
| C、物质B的质量分数减小了 |
| D、a>b |
在用锌片、铜片和稀硫酸组成的原电池装置中,经过-段时间工作后,下列说法正确的是( )
| A、锌片是正极,铜片是负极 |
| B、电子是从锌片通过导线流到铜片上 |
| C、溶液中H+移向锌片被还原变成H2 |
| D、电解液的pH逐渐变小 |
下列溶液中,一定能大量共存的微粒组是( )
| A、室温下,pH=1的溶液中:Na+、Fe2+、NO-3、SO42- |
| B、由水电离的c(H+)=1×10-13 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C、含有大量Fe3+的溶液中:Al3+、Cu2+、Cl-、SO42- |
| D、c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO42-、SCN- |