题目内容
下列溶液中,一定能大量共存的微粒组是( )
| A、室温下,pH=1的溶液中:Na+、Fe2+、NO-3、SO42- |
| B、由水电离的c(H+)=1×10-13 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C、含有大量Fe3+的溶液中:Al3+、Cu2+、Cl-、SO42- |
| D、c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO42-、SCN- |
考点:离子共存问题
专题:离子反应专题
分析:A.pH=1的溶液,显酸性,离子之间发生氧化还原反应;
B.由水电离的c(H+)=1×10-13 mol/L的溶液,为酸或碱溶液;
C.该组离子之间不反应;
D.离子之间结合生成络离子.
B.由水电离的c(H+)=1×10-13 mol/L的溶液,为酸或碱溶液;
C.该组离子之间不反应;
D.离子之间结合生成络离子.
解答:
解:A.pH=1的溶液,显酸性,H+、Fe2+、NO3-发生氧化还原反应,不能大量共存,故A错误;
B.由水电离的c(H+)=1×10-13 mol/L的溶液,为酸或碱溶液,HCO3-与酸、碱均反应,一定不能共存,故B错误;
C.该组离子之间不反应,可大量共存,故C正确;
D.Fe3+、SCN-结合生成络离子,不能大量共存,故D错误;
故选C.
B.由水电离的c(H+)=1×10-13 mol/L的溶液,为酸或碱溶液,HCO3-与酸、碱均反应,一定不能共存,故B错误;
C.该组离子之间不反应,可大量共存,故C正确;
D.Fe3+、SCN-结合生成络离子,不能大量共存,故D错误;
故选C.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应、络合反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
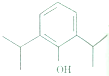 2009年8月25日洛杉矶首席验尸官在休斯顿法庭上公布流行音乐天王杰克逊被注射异丙酚,“天王星”就此陨落.异丙酚是一种强力的镇静剂,常被麻痹医生称为“牛奶”.其结构如图所示,下列有关异丙酚的说法不正确的是( )
2009年8月25日洛杉矶首席验尸官在休斯顿法庭上公布流行音乐天王杰克逊被注射异丙酚,“天王星”就此陨落.异丙酚是一种强力的镇静剂,常被麻痹医生称为“牛奶”.其结构如图所示,下列有关异丙酚的说法不正确的是( )| A、能发生加成反应 |
| B、能和FeCl3溶液发生显色反应 |
| C、能与Na2CO3溶液发生反应 |
| D、分子中所有碳原子都在同一平面上 |
不属于离子反应(在水溶液中进行的复分解类型的离子反应)发生的条件是( )
| A、生成沉淀 |
| B、生成弱电解质 |
| C、生成气体 |
| D、生成强电解质 |
下列各组中的两种物质相互作用时,反应条件(温度、反应物用量比)改变,不会引起产物的种类改变的是( )
| A、Al和 NaOH溶液 |
| B、NaOH溶液和AlCl3溶液 |
| C、Na和O2 |
| D、NaOH溶液和CO2 |
NA表示阿伏加德罗常数,以下各物质所含分子数最少的是( )
| A、含2NA个氢分子的氢气 |
| B、17g氨气(NH3的摩尔质量为17g?mol-l) |
| C、0.8mol氧气 |
| D、标准状况下11.2 L氯气 |
下列变化中,需加入适当的氧化剂才能完成的是( )
| A、Fe→FeCl3 |
| B、CuO→Cu |
| C、Cl2→HClO |
| D、SiO2→Na2SiO3 |
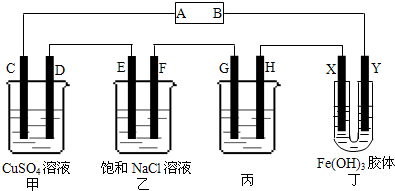
 (1)用l体积SO2和3体积空气混合,在450℃以上通过V2O5催化剂,发生如下反应:2SO2(g)+O2(g)?2SO3(g).一段时间后达到平衡,若此时同温同压下测得反应前后混合气体的密度比为0.9:1,则SO2平衡转化率为
(1)用l体积SO2和3体积空气混合,在450℃以上通过V2O5催化剂,发生如下反应:2SO2(g)+O2(g)?2SO3(g).一段时间后达到平衡,若此时同温同压下测得反应前后混合气体的密度比为0.9:1,则SO2平衡转化率为